Ihre wesentliche GLP-Checklisten-Vorlage: Ein praktischer Leitfaden
Veröffentlicht: 09/01/2025 Aktualisiert: 03/19/2026
Inhaltsverzeichnis
- Einleitung: Warum eine GLP-Checkliste wichtig ist
- Das Verständnis der Kernprinzipien der GLP
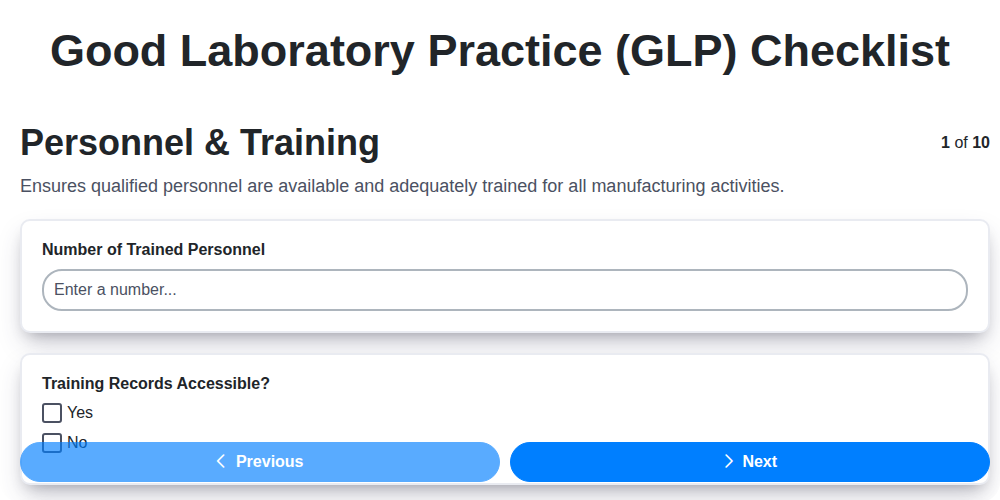
- Abschnitt 1: Personal und Schulung - Aufbau eines qualifizierten Teams
- Abschnitt 2: Einrichtungen und Ausrüstung - Gewährleistung einer kontrollierten Umgebung
- Abschnitt 3: Materialwirtschaft - Rückverfolgbarkeit gewährleisten
- Abschnitt 4: SOPs und Verfahren - Das Fundament für Konsistenz
- Abschnitt 5: Datenintegrität & Dokumentation: Ein kritischer Schwerpunkt
- Abschnitt 6: Qualitätskontrolle & Testen - Ihre Ergebnisse bestätigen
- Abschnitt 7: Umgang mit Abweichungen & Untersuchungen - Lernen aus Fehlern
- Abschnitt 8: Änderungsmanagement: Effektives Management von Änderungen
- Abschnitt 9: Qualifizierung und Validierung der Ausrüstung - Leistungsnachweis
- Abschnitt 10: Prozessvalidierung: Gewährleistung der Reproduzierbarkeit
- Die Umsetzung Ihrer GLP-Checklistenvorlage
- Ressourcen & Links
Kurz gesagt: Müssen Sie sicherstellen, dass Ihr Labor die Vorgaben der Guten Laborpraxis (GLP) erfüllt? Dieser Leitfaden bietet eine praktische Checklistenvorlage, die alles abdeckt - von Personalschulungen und Instandhaltung der Einrichtung bis hin zu Datenmanagement und -validierung. Laden Sie sie herunter, passen Sie sie an Ihre Prozesse an und nutzen Sie sie, um die Einhaltung systematisch zu verfolgen und die Datenintegrität zu gewährleisten!
Einleitung: Warum eine GLP-Checkliste wichtig ist
In der Welt der wissenschaftlichen Forschung und Produktentwicklung ist Datenintegrität nicht nur wünschenswert - sie ist das Fundament für Glaubwürdigkeit und Compliance. Die Richtlinien für die Guten Laborpraxis (GLP) sollen sicherstellen, dass erzeugte Daten zuverlässig, nachvollziehbar und verteidigbar sind. Aber das Wissen über diePrinzipienDie Einhaltung der GLP ist nur die halbe Miete. Eine konsistente Anwendung, sorgfältige Dokumentation und ein wachsames Auge für Details sind entscheidend, um eine echte GLP-Konformität zu erreichen. Hier wird eine gut strukturierte GLP-Checkliste zu einem unschätzbaren Hilfsmittel. Sie ist mehr als nur eine Aufgabenliste - eine GLP-Checkliste bietet Ihrem Labor einen klaren Fahrplan, fördert eine Kultur der Verantwortlichkeit und minimiert das Risiko kostspieliger Fehler oder regulatorischer Rückschläge. Betrachten Sie sie als die Gewissheit Ihres Labors, dass jeder Prozess, jede Beobachtung und jedes Ergebnis dokumentiert, validiert und letztendlich vertrauenswürdig ist.
Das Verständnis der Kernprinzipien der GLP
GLP ist nicht nur eine Liste von Regeln; es ist eine Philosophie, die auf einigen Schlüsselprinzipien basiert. Im Kern steht das unerschütterliche Bekenntnis zur Datensicherheit - die Gewährleistung von Genauigkeit, Zuverlässigkeit und Nachvollziehbarkeit der Daten. Dies geht über die bloße Dokumentation von Beobachtungen hinaus; es erfordert sorgfältige Detailgenauigkeit, die Einhaltung etablierter Verfahren und ein System von Kontrollen und Abwägung.
Mehrere Kernprinzipien bilden die Grundlage für dieses Engagement.PlanungDie Priorität ist oberstes Gebot. Ein klar definiertes Protokoll, das die Ziele, die Methodik und die statistische Analyse der Studie darlegt, bildet das Fundament.Auftrittbezieht sich auf die konsequente Ausführung des Protokolls durch geschultes Personal.Dokumentationist das Fundament von GLP - jede Handlung, jede Beobachtung und jede Berechnung muss klar und zeitnah dokumentiert werden.Qualitätssicherungist die unabhängige Stelle, die die Einhaltung der GLP-Richtlinien überprüft und somit eine entscheidende Schutzfunktion gegen Fehler und Nichteinhaltung darstellt. Abschließend,Archivierunggarantiert eine langfristige Datensicherung und -verfügbarkeit für Audits und zukünftige Referenzen. Die Anerkennung und Einhaltung dieser Grundsätze bildet das Fundament für die Generierung vertrauenswürdiger wissenschaftlicher Daten und die Erreichung echter GLP-Konformität.
Abschnitt 1: Personal und Schulung - Aufbau eines qualifizierten Teams
Der Erfolg eines Labors hängt von der Expertise und der Kompetenz seiner Mitarbeiter ab. Die Einhaltung der GLP-Richtlinien geht über Verfahren und Ausrüstung hinaus; sie basiert grundlegend auf einem qualifizierten Team, das über das Wissen und die Fähigkeiten verfügt, seine Aufgaben präzise und ethisch korrekt auszuführen. Dies beginnt mit sorgfältiger Auswahl und erstreckt sich auf kontinuierliche Schulungen und Leistungsbeurteilungen.
Jenseits der Qualifikationen: Kompetenz bewerten
Auch wenn formale Bildung und Erfahrung wichtig sind, ist eine gründliche Beurteilung praktischer Fähigkeiten entscheidend. Einstellungspersonal sollte Bewerber priorisieren, die ein fundiertes Verständnis der GLP-Prinzipien und ein Engagement für die Datenintegrität zeigen. Diese Beurteilung kann praktische Demonstrationen, fallbezogene Interviews und Bewertungen der Problemlösungsfähigkeiten umfassen. Es sollten kompetenzbasierte Bewertungen in Bezug auf spezifische Tätigkeitsbereiche in Betracht gezogen werden.
Der Lernweg: Von der Einarbeitung zur kontinuierlichen Verbesserung
Die erstmalige Einarbeitungsschulung muss die Grundlagen von GLP, spezifische SOPs (Standardarbeitsanweisungen) in Bezug auf die jeweilige Rolle und wichtige Sicherheitsvorkehrungen umfassen. Dies sollte eine Überprüfung der Erwartungen an die Datenintegrität und die Bedeutung einer korrekten Dokumentation beinhalten. Schulungsnachweisemusssorgfältig gepflegt werden, wobei die behandelten Inhalte, die Trainingsdaten sowie die Namen der Trainer und Teilnehmer dokumentiert werden.
Kontinuierliche Kompetenzentwicklung - Ein Bekenntnis zur Weiterentwicklung
Die Schulung sollte keine einmalige Veranstaltung sein. Ein umfassendes Programm beinhaltet regelmäßige Auffrischungskurse, Updates zu regulatorischen Änderungen sowie Schulungen zu neuen Technologien oder Methoden. Berücksichtigen Sie die Integration von Querschnittsschulungen, um die Kompetenzen der Mitarbeiter zu erweitern und ihre Flexibilität zu erhöhen. Leistungsbeurteilungen sollten eine Bewertung der Einhaltung der GLP sowie die Identifizierung von Bereichen zur fachlichen Weiterentwicklung beinhalten. Eine Kultur des kontinuierlichen Lernens befähigt Ihr Team, die höchsten Standards von Qualität und Compliance aufrechtzuerhalten.
Abschnitt 2: Einrichtungen und Ausrüstung - Gewährleistung einer kontrollierten Umgebung
Das Fundament für verlässliche Daten beginnt mit einer penibel kontrollierten Umgebung. Räumlichkeiten und Ausrüstung spielen eine entscheidende Rolle bei der Wahrung der Datenintegrität, und ein proaktiver Ansatz bei deren Verwaltung ist von größter Bedeutung. Es geht dabei nicht nur um Sauberkeit; es geht darum, kontrollierte Bedingungen zu gewährleisten, die Variabilität und potenzielle Fehlerquellen minimieren.
Ein robuster Abschnitt für Einrichtungen und Geräte in Ihrer GLP-Checkliste sollte mehrere Schlüsselbereiche berücksichtigen. Zunächst sollte das physikalische Layout betrachtet werden. Gibt es ausreichend Platz, um alle notwendigen Verfahren sicher und effizient durchzuführen? Die Trennung unverträglichen Materials ist unerlässlich - die Verhinderung versehentlicher Kontamination ist ein entscheidendes Präventionsmaß. Belüftungssysteme müssen regelmäßig inspiziert und gewartet werden, um eine ordnungsgemäße Luftqualität und die Entfernung potenziell schädlicher Dämpfe zu gewährleisten.
Temperatur- und Feuchtigkeitskontrolle sind oft unerlässlich, insbesondere für empfindliche Proben oder Reagenzien. Dokumentierte Umweltüberwachungsprogramme, einschließlich regelmäßiger Protokollierung und Kalibrierung von Temperatur- und Feuchtigkeitssensoren, sind entscheidend.
Was die Ausrüstung betrifft, ist ein systematischer Ansatz erforderlich. Jedes in GLP-bezogenen Tätigkeiten verwendete Gerät muss gemäß einem dokumentierten Zeitplan ordnungsgemäß gewartet und kalibriert werden. Aufzeichnungen über diese Aktivitäten, einschließlich Daten, Ergebnissen und beteiligtem Personal, sind unerlässlich. Neben der routinemäßigen Wartung sollten für kritische Geräte die Installation qualifizierung (IQ), die Betrieb qualifizierung (OQ) und die Leistungs qualifizierung (PQ) durchgeführt und dokumentiert werden, um sicherzustellen, dass sie korrekt installiert sind, wie vorgesehen funktionieren und konsistent arbeiten. Schließlich muss ein System zur Verwaltung von nicht konformen Geräten - d. h. Geräten, die außer Betrieb sind oder repariert werden müssen - vorhanden sein, um deren unautorisierte Verwendung zu verhindern.
Abschnitt 3: Materialwirtschaft - Rückverfolgbarkeit gewährleisten
Eine effektive Materialverwaltung bildet das Fundament der GLP-Konformität und wirkt sich direkt auf die Datenintegrität und Reproduzierbarkeit aus. Es geht nicht nur um die Lagerung von Chemikalien, sondern um die Erstellung einer nachvollziehbaren Dokumentation für jedes im Rahmen Ihrer Studien verwendete Material. Das bedeutet sorgfältige Aufzeichnungen von dem Zeitpunkt, an dem ein Material in das Labor gelangt, bis zu seiner Entsorgung oder Verwendung in einem Endprodukt.
Schlüsselkomponenten der Rückverfolgbarkeit:
- Umfassende Bestandsaufzeichnungen: Ein solides Bestandsverwaltungssystem ist unerlässlich. Es sollte Details wie Lieferanteninformationen, Chargennummern, Datum des Eingangs, Verfallsdatum, empfangene Menge und Lagerort im Labor enthalten. Digitale Systeme werden für Effizienz und Genauigkeit dringend empfohlen.
- Eindeutige Kennzeichnung: Jeder Behälter mit Material sollte eindeutig identifiziert werden, typischerweise durch Etikettierung. Die Etiketten sollten den Materialnamen, die Konzentration, die Chargennummer, das Öffnungsdatum und die Initialen der Person, die ihn geöffnet hat, enthalten.
- Kontrollierter Zugang: Beschränken Sie den Zugang zu Lagerbereichen auf befugtes Personal. Dies minimiert das Risiko einer unbefugten Nutzung oder Kontamination.
- Verbleibende Proben: Bewahren Sie repräsentative Proben jeder Materialcharge, die in GLP-Studien verwendet wird, auf. Diese Proben müssen ordnungsgemäß beschriftet und gelagert werden, wobei deren Integrität zu gewährleisten ist. Sie sind von entscheidender Bedeutung für zukünftige Referenzen, Nachuntersuchungen oder Ermittlungen.
- Materialverbrauchslisten: Führen Sie detaillierte Protokolle, die die Verwendung jedes Materials in bestimmten Studien oder Experimenten dokumentieren. Diese Protokolle sollten das Datum, die verwendete Menge, die Studienummer und die Initialen der Person, die das Material verwendet hat, enthalten.
- Regelmäßige Prüfungen: Führen Sie regelmäßige Audits Ihres Materialwirtschaftssystems durch, um Abweichungen oder Schwächen zu identifizieren und zu beheben. Dies umfasst die Überprüfung der Richtigkeit der Aufzeichnungen, die sachgerechte Lagerung der Materialien und die Überwachung von Verfallsdaten.
Effektives Materialmanagement ist nicht nur eine prozedurale Anforderung, sondern ein wichtiger Schutzmechanismus, der die Integrität Ihrer Daten und die Glaubwürdigkeit Ihrer Forschung sichert.
Abschnitt 4: SOPs und Verfahren - Das Fundament für Konsistenz
Standardarbeitsanweisungen (SOPs) sind nicht nur Papierkram; sie bilden das Fundament für reproduzierbare Ergebnisse und sind ein Beweis für das Qualitätsengagement Ihres Labors. Betrachten Sie sie als das kollektive Gedächtnis Ihres Labors, das dokumentiertwieDie Aufgaben werden stets einheitlich und jedes Mal durchgeführt. Ohne solide SOPs schleichen Abweichungen ein, Daten werden unzuverlässig und die Einhaltung wird zu einem ständigen Kampf.
Effektive SOPs gehen über einfache Schritt-für-Schritt-Anleitungen hinaus. Sie sollten den Zweck des Verfahrens klar definieren, verantwortliche Personen benennen, benötigte Ausrüstung und Materialien spezifizieren, Sicherheitsvorkehrungen umreißen und erwartete Ergebnisse detailliert beschreiben. Sie sind keine statischen Dokumente; sie bedürfen regelmäßiger Überprüfung und Aktualisierung, um Änderungen in Prozessen, Technologien oder gesetzlichen Anforderungen widerzuspiegeln.
Entscheidend ist, dass SOPs nur so gut sind wie die damit verbundene Schulung. Die Überprüfung des Verständnisses, beispielsweise durch praktische Demonstrationen oder Bewertungen, ist unerlässlich, um sicherzustellen, dass alle Mitarbeiter die Verfahren korrekt befolgen. Regelmäßige Audits der SOP-Einhaltung sind ebenfalls entscheidend, um Bereiche für Verbesserungen zu identifizieren und eine Kultur der Compliance zu stärken. Ein gut gepflegtes und aktiv genutztes SOP-Programm geht nicht nur darum, Anforderungen abzuhaken - es geht darum, eine Grundlage wissenschaftlicher Genauigkeit und Datenintegrität zu schaffen.
Abschnitt 5: Datenintegrität & Dokumentation: Ein kritischer Schwerpunkt
Die Datenintegrität ist das Fundament der GLP-Konformität, und eine solide Dokumentation ist ihre praktische Umsetzung. Es geht nicht nur darum festzuhalten, was passiert ist, sondern darum sicherzustellen, dass diese Aufzeichnungen korrekt, vollständig, konsistent, dauerhaft und zugänglich sind. Beeinträchtigte Datenintegrität kann schwerwiegende Folgen haben, von behördlichen Sanktionen bis hin zu ungültigen Forschungsergebnissen.
Dieser Abschnitt konzentriert sich auf wesentliche Praktiken zur Wahrung der Datenintegrität und sorgfältiger Dokumentation.
- Originaldaten sind von größter Bedeutung.Alle Rohdaten, die im Rahmen einer GLP-Studie generiert werden - seien es Druckerzeugnisse von Messgeräten, handschriftliche Notizen oder elektronische Aufzeichnungen -mussdie ursprüngliche Aufzeichnung sein. Das bedeutet, dass keine Daten überschrieben, gelöscht oder verändert werden dürfen. Falls Korrekturen notwendig sind, müssen diese mit einer datums- und initialsierter Nachtragung erfolgen, die eindeutig auf den ursprünglichen Eintrag Bezug nimmt.
- Prüfpfade für elektronische Dokumente: Bei der Nutzung elektronischer Systeme ist sicherzustellen, dass umfassende Prüfprotokolle aktiviert und ordnungsgemäß funktionieren. Diese Protokolle sollten jede im System durchgeführte Aktion erfassen, einschließlich Dateneingabe, -änderung und -löschung. Überprüfen Sie die Prüfprotokoll-Protokolle regelmäßig, um eventuelle Anomalien zu identifizieren.
- Sichere Datenspeicherung & Zugriffskontrolle: Implementieren Sie robuste Zugriffskontrollen, um den Datenzugriff auf autorisierte Personen zu beschränken. Verwenden Sie sichere Aufbewahrungsmethoden (sowohl physisch als auch elektronisch), um Daten vor Verlust, Diebstahl oder unbefugter Veränderung zu schützen.
- Datenspeicherungspolitik: Definieren Sie klare Richtlinien zur Datenaufbewahrung, die den behördlichen Anforderungen und den internen Vorgaben entsprechen. Diese Richtlinien sollten festlegen, wie lange Aufzeichnungen aufbewahrt werden müssen und wie sie archiviert werden.
- Klare Kennzeichnung und Indizierung: Stellen Sie sicher, dass alle Aufzeichnungen klar gekennzeichnet und indiziert sind, um eine einfache Auffindbarkeit und Rückverfolgbarkeit zu gewährleisten. Dies ist insbesondere bei physischen Aufzeichnungen wichtig.
- Chronologische ReihenfolgeFühren Sie Aufzeichnungen in strikter chronologischer Reihenfolge, um eine genaue Darstellung des Studienfortschritts zu gewährleisten.
- Schulung & Sensibilisierung: Schulen Sie das Personal regelmäßig in Bezug auf Prinzipien der Datenintegrität und bewährten Verfahren zur Dokumentation. Eine Kultur der Sensibilisierung ist entscheidend, um unbeabsichtigte Fehler zu vermeiden.
Abschnitt 6: Qualitätskontrolle & Testen - Ihre Ergebnisse bestätigen
Qualitätskontrolle (QC) und Tests bilden das Fundament für zuverlässige Daten in jedem GLP-konformen Labor. Es reicht nicht aus, einfachauftretenTests; Sie müssen rigoros validieren, dass diese Tests korrekt, präzise und durchgehend zuverlässige Ergebnisse liefern. Dieser Abschnitt befasst sich mit den wichtigsten Aspekten für robuste Qualitätssicherungs- und Testverfahren.
Methodenvalidierung: Das Fundament des Vertrauens
Bevor eine analytische Methode für GLP-bezogene Studien eingesetzt wird,musswerden validiert. Die Validierung belegt, dass die Methode für ihren Verwendungszweck geeignet ist. Dies beinhaltet typischerweise die Bewertung von Parametern wie:
- Genauigkeit: Wie nahe das Testergebnis am tatsächlichen Wert liegt.
- PräzisionDie Wiederholbarkeit und Reproduzierbarkeit der Ergebnisse. (Berücksichtigen Sie dabei die Wiederholbarkeit innerhalb eines einzelnen Durchlaufs und die Reproduzierbarkeit über verschiedene Analysten, Instrumente und Tage hinweg.)
- Spezifität/SelektivitätDie Fähigkeit der Methode, nur das Zielanalyten ohne Störfaktoren zu messen.
- Nachweisgrenze (NG): Die niedrigste Konzentration des Analyten, die nachweisbar ist.
- Bestimmungsgrenze (BGN)Die niedrigste Analytenkonzentration, die zuverlässig quantifiziert werden kann.
- LinearitätDer Bereich, über den die Methode proportional genaue Ergebnisse liefert.
- RobustheitDie Fähigkeit der Methode, kleinen Schwankungen der Bedingungen (z. B. Temperatur, pH-Wert) standzuhalten.
Validierungsstudien werden sorgfältig dokumentiert, und Akzeptanzkriterien sind eindeutig definiert.vorDie Tests beginnen. Abweichungen von diesen Kriterien müssen untersucht und behoben werden, bevor die Methode als validiert gelten kann.
Laufende Qualitätskontrolle - Über die erste Validierung hinaus
Validierung ist kein einmaliges Ereignis. Kontinuierliche Qualitätskontrolle (QK) ist unerlässlich, um die Datenintegrität zu gewährleisten. Dazu gehören:
- Kontrollproben: Laufkontrollen mit bekannten Konzentrationen zusammen mit den Untersuchungsproben durchführen, um die Leistung des Analyseinstruments zu überwachen. Diese sollten repräsentativ für die Matrix und die Analyten sein, die geprüft werden.
- Kalibrierungskurven: Regelmäßige Erstellung und Validierung von Kalibrierungskurven unter Verwendung von Standards bekannter Konzentrationen.
- Gerätewartung: Die Einführung eines präventiven Wartungsplans für alle Analysegeräte zur Sicherstellung des ordnungsgemäßen Funktionierens.
- Reagenzien- und Standardmanagement: Die Lagerung, Handhabung und Ablaufdaten von Reagenzien und Standards streng kontrollieren.
- Datenprüfung: Gründliche Überprüfung aller Rohdaten und Ergebnisse, um etwaige Anomalien oder Trends zu identifizieren, die auf ein Problem hindeuten könnten.
Durch die Priorisierung strenger Qualitätskontroll- und Testverfahren schaffen Sie eine Grundlage für Vertrauen in Ihre Daten, gewährleisten die Einhaltung von Vorschriften und erhöhen die Glaubwürdigkeit Ihrer Forschungsergebnisse.
Abschnitt 7: Umgang mit Abweichungen & Untersuchungen - Lernen aus Fehlern
Abweichungen sind ein unvermeidlicher Bestandteil jeder Laborarbeit. Sie stellen Fälle dar, in denen Verfahren nicht exakt gemäß den SOPs befolgt wurden, unerwartete Ergebnisse auftraten oder Geräte versagten. Das bloße Auftreten einer Abweichung muss jedoch keine Ursache zur Besorgnis sein; es ist dieUmgangvon dieser Abweichung, die wirklich relevant ist. Ein robuster Prozess zur Abweichungsverarbeitung geht nicht darum, Schuld zuzuweisen; es geht darum, Verbesserungspotenziale zu identifizieren und eine Wiederholung zu verhindern.
Ein strukturierter Ansatz zur Abweichungsverarbeitung sollte mehrere Schlüsselschritte umfassen. Zuerst,Erfassung und DokumentationDie Einhaltung ist von größter Bedeutung. Jegliche Abweichungen, unabhängig von ihrem vermeintlichen Ausmaß, müssen umgehend dokumentiert werden. Diese Dokumentation sollte eine klare Beschreibung des Vorfalls, des Zeitpunkts, der beteiligten Personen und möglicher Auswirkungen auf die Datensicherheit enthalten.
Als Nächstes eine gründlicheErmittlungsollte eingeleitet werden. Das geht über die bloße Feststellung der Abweichung hinaus; es erfordert eine tiefergehende Analyse derUrsachenforschung War es ein Schulungsdefizit? Ein fehlerhaftes SOP? Ein Geräteausfall? Ein systemisches Prozessproblem? Der Einsatz von Werkzeugen wie der 5-Warum-Methode kann unschätzbar wertvoll sein, um das zugrunde liegende Problem aufzudecken.
Sobald die Ursache identifiziert ist, eineKorrekturmaßnahmen und präventive Maßnahmen (CAPA)Der Plan sollte entwickelt und umgesetzt werden. Korrekturmaßnahmen beheben das unmittelbare Problem, um dessen Wiederholung imgleichDie Präventivmaßnahmen zielen auf die Ursache ab, um zu verhindern, dass ähnliche Probleme in Zukunft auftreten.andererBereiche des Labors.
Es ist entscheidend, dass der gesamte Abweichungsverarbeitungsprozess sorgfältig dokumentiert wird. Dazu gehören der ursprüngliche Abweichungsmeldung, die Untersuchungsergebnisse, der CAPA-Plan und die Verifizierung, dass die korrigierenden und präventiven Maßnahmen wirksam waren. Diese Dokumentation dient als wertvolle Prüfspur und unterstreicht das Engagement für kontinuierliche Verbesserung. Bedenken Sie, dass eine Abweichung kein Versagen ist; sie ist eine Lernmöglichkeit - eine Chance, die Prozesse Ihres Labors zu stärken und die Zuverlässigkeit Ihrer Daten zu erhöhen.
Abschnitt 8: Änderungsmanagement: Effektives Management von Änderungen
Veränderungen sind in jeder Laborumgebung unvermeidlich. Ob es sich um eine Aktualisierung einer SOP, ein neues Gerät oder eine Änderung eines Studienprotokolls handelt, das effektive Management dieser Veränderungen ist entscheidend für die Aufrechterhaltung der GLP-Konformität und der Datensicherheit. Ein robustes Änderungskontrollsystem stellt sicher, dass Änderungen gründlich bewertet, dokumentiert und kontrolliert umgesetzt werden, wodurch potenzielle Risiken minimiert und die Zuverlässigkeit Ihrer Daten erhalten bleibt.
Das Herzstück eines erfolgreichen Change-Management-Systems ist ein dokumentiertes Verfahren. Dieses Verfahren sollte die Schritte zur Initiierung einer Änderungsanfrage, die Durchführung einer Risikobewertung zur Einschätzung der potenziellen Auswirkungen, die Einholung der erforderlichen Genehmigungen, die Umsetzung der Änderung und die Verifizierung ihrer Wirksamkeit umfassen. Entscheidend ist dabei, festzulegen, wer die Befugnis hat, Änderungen zu initiieren, zu prüfen und zu genehmigen.
Nicht alle Änderungen erfordern die gleiche Prüfung. Ihr System sollte Änderungen anhand ihres potenziellen Risikoniveaus - gering, moderat und erheblich - kategorisieren und entsprechende Anforderungen an Überprüfung und Dokumentation zuweisen. So könnte beispielsweise eine geringfügige Tippfehlerkorrektur in einer SOP eine einfache Genehmigung und Dokumentation erfordern, während eine wesentliche Änderung eines Herstellungsprozesses eine umfassende Validierungsstudie notwendig machen würde.
Über die unmittelbare Änderung selbst hinaus, berücksichtigen Sie die daraus resultierenden Auswirkungen. Änderungen in einem Bereich können oft andere beeinflussen. Ihre Risikobewertung sollte diese potenziellen Folgeeffekte proaktiv identifizieren und Minderungsstrategien beinhalten. Auch eine angemessene Schulung ist unerlässlich; Mitarbeiter müssen über Änderungen informiert sein und verstehen, wie diese ihre Aufgaben und Verantwortlichkeiten beeinflussen. Schließlich vergessen Sie nicht, Ihre Änderungsprozesskontrolle selbst regelmäßig zu überprüfen, um deren Wirksamkeit und Relevanz für Ihre sich entwickelnden Laborabläufe sicherzustellen.
Abschnitt 9: Qualifizierung und Validierung der Ausrüstung - Leistungsnachweis
Die Qualifizierung und Validierung von Geräten geht über das Abhaken von Punkten hinaus; es geht um einen nachweislichen Beweis dafür, dass Ihre Geräte konsistent wie vorgesehen funktionieren und zuverlässige Daten liefern. Es handelt sich um einen vielschichtigen Prozess, der darauf abzielt, Vertrauen in jedes Experiment und jedes Ergebnis zu schaffen.
Der Qualifizierungsprozess umfasst in der Regel drei entscheidende Phasen:
- Installationsqualifizierung (IQ): Dies bestätigt, dass die Ausrüstung gemäß den Herstellerangaben korrekt installiert und ordnungsgemäß an Versorgungseinrichtungen wie Strom, Wasser und Gas angeschlossen wurde. Die Dokumentation enthält Seriennummern, Installationsdaten und Angaben zum Lieferanten.
- Betriebliche Qualifizierung (BQ)Diese Phase zeigt, dass die Ausrüstung gemäß den Herstellerangaben unter definierten Betriebsbedingungen funktioniert. Dies beinhaltet häufig Leistungstests über eine Reihe von Parametern. Die Akzeptanzkriterien sind vorgegeben und müssen erfüllt werden.
- Qualifizierung der Leistung (oder: Leistungskualifizierung)Dies ist der letzte Schritt, der bestätigt, dass die Ausrüstung bei Verwendung für ihren vorgesehenen Zweck innerhalb der spezifischen Laborumgebung konsistent nach den festgelegten Akzeptanzkriterien funktioniert. Er validiert im Wesentlichen, dass die Leistung der Ausrüstung zuverlässig und reproduzierbar ist.
Die Validierung beschränkt sich nicht nur auf die Ausrüstung. Analytische Methoden, Software zur Datenerfassung und -analyse sowie ganze Prozesse müssen ebenfalls validiert werden, um ihre Richtigkeit, Zuverlässigkeit und Eignung für die Einhaltung der GLP-Anforderungen sicherzustellen. Dies erfordert dokumentierte Belege dafür, dass die Methode/Software/der Prozess bei Verwendung gemäß vordefinierten Verfahren konsistent die erwarteten Ergebnisse liefert.
Es ist entscheidend, dass Qualifizierungs- und Validierungsdokumentationen sorgfältig gepflegt, jederzeit zugänglich und regelmäßig überprüft werden, um die fortlaufende Konformität sicherzustellen. Jegliche Abweichungen oder Fehler müssen gründlich untersucht und dokumentiert werden, wobei die umgesetzten Korrekturmaßnahmen zu verifizieren sind. Ziel ist nicht nur eine einmalige Qualifizierung und Validierung, sondern die Etablierung eines Systems für fortlaufende Sicherheit und kontinuierliche Verbesserung.
Abschnitt 10: Prozessvalidierung: Gewährleistung der Reproduzierbarkeit
Prozessvalidierung ist nicht nur eine wünschenswerte Ergänzung; sie ist ein Eckpfeiler der GLP und ein entscheidender Nachweis Ihrer Fähigkeit, zuverlässige Daten oder Produkte konsistent zu produzieren. Sie geht über die bloße Befolgung einer Prozedur hinaus - es geht darum, zu beweisen, dass der ProzessimmerFunktioniert unter definierten Bedingungen wie erwartet. Dies beinhaltet typischerweise den Nachweis, dass der Prozess innerhalb vorab festgelegter Akzeptanzkriterien konsistent arbeitet.
Es gibt drei primäre Phasen der Prozessvalidierung: Prozessdesignvalidierung,ProzessqualifizierungundKontinuierliche Prozessverifizierung (KPV) Please provide the English text you want me to translate.
- Prozessdesignvalidierung: Diese Phase konzentriert sich auf die Bestätigung, dass das Prozessdesign robust und in der Lage ist, das gewünschte Ergebnis zu erzielen. Dies wird häufig durch umfassende Risikobewertungen, Simulationen und Pilotstudien erreicht. Diese Stufe legt die Basis für Ihren Prozess und dessen erwartete Leistung fest.
- Prozessqualifizierung: Sobald das Design validiert ist, verifiziert die Prozessqualifizierung, dass der Prozess unter tatsächlichen Betriebsbedingungen konsistent ausgeführt wird. Dies beinhaltet die Durchführung mehrerer Validierungsdurchläufe unter sorgfältig kontrollierten Parametern, die akribische Dokumentation der Ergebnisse und den Nachweis, dass alle Akzeptanzkriterien erfüllt sind.
- Kontinuierliche Prozessverifizierung (KPV): CPV ist eine kontinuierliche Bewertung des validierten Prozesses. Sie beinhaltet die regelmäßige Überwachung kritischer Prozessparameter (CPPs) und kritischer Qualitätsmerkmale (CQAs), um die Prozesskontrolle aufrechtzuerhalten und mögliche Abweichungen zu identifizieren, die einer Untersuchung bedürfen. Statistische Prozessregelungen (SPC) werden häufig im CPV eingesetzt, um Prozessentwicklungen zu verfolgen und bei Bedarf Warnmeldungen auszulösen.
Eine robuste Prozessvalidierung unterstreicht Ihr Engagement für die Datensicherheit, reduziert das Risiko von Produktfehlern und stärkt Ihre Compliance-Position gegenüber den Aufsichtsbehörden. Sorgfältige Dokumentation über den gesamten Validierungszyklus ist entscheidend für die Vorbereitung auf Audits und die Rückverfolgbarkeit.
Die Umsetzung Ihrer GLP-Checklistenvorlage
Eine statische Prüfliste, selbst wenn sie noch so umfassend ist, ist lediglich ein Ausgangspunkt. Echte GLP-Konformität erfordert einen dynamischen, proaktiven Ansatz. Hier erfahren Sie, wie Sie über ein Dokument hinausgehen und Ihre Prüfliste aktiv in den täglichen Betrieb integrieren können:
1. Verantwortlichkeit zuweisen und festlegen: Lassen Sie Ihre Checkliste nicht verstauben. Übertragen Sie jedem Abschnitt konkrete Personen oder Teams als Verantwortliche. Dies stellt sicher, dass jemand die Überwachung, Aktualisierung und die Bearbeitung aller festgestellten Probleme aktiv übernimmt. Klare Verantwortlichkeit fördert das Verantwortungsbewusstsein und unterstützt kontinuierliche Verbesserungen.
2. In Arbeitsabläufe integrieren: Integrieren Sie Prüflisten-Punkte nahtlos in bestehende Laborabläufe. Betrachten Sie es nicht als Ergänzung, sondern als integralen Bestandteil der Aufgabenbearbeitung. Beispielsweise können Prüfschritte innerhalb von SOPs (Standardarbeitsanweisungen) aufgenommen oder digitale Prüflisten in LIMS (Laboratory Information Management Systems) integriert werden.
4. Regelmäßige Überprüfungszyklen durchführen: Planen Sie regelmäßige Überprüfungszyklen (wöchentlich, monatlich, vierteljährlich), um die Einhaltung der Checkliste systematisch zu bewerten. Diese Überprüfungen sollten nicht den Charakter von Strafmaßnahmen haben; sie bieten stattdessen Gelegenheiten zum Lernen, zur Identifizierung von Prozessengpässen und zur Stärkung der GLP-Praktiken.
4. Digitale Werkzeuge nutzen: Nutzen Sie die Technologie! Digitale Checklisten-Vorlagen, die mit Datenanalysen integriert sind, können Erinnerungen automatisieren, die Leistung verfolgen und sofort Bereiche hervorheben, die Aufmerksamkeit erfordern. Dies geht über manuelle Prozesse hinaus und liefert Echtzeit-Einblicke.
5. Fördern Sie eine Kultur der offenen Kommunikation: Ermutigen Sie die Teammitglieder, Abweichungen oder Bedenken proaktiv zu identifizieren und zu melden. Eine Kultur ohne Schuldzuweisung ist entscheidend; der Fokus sollte auf dem Lernen aus Fehlern und der Verbesserung von Prozessen liegen. Machen Sie die Checkliste zu einem Werkzeug für gemeinsames Wachstum, nicht zu einer Quelle der Angst.
6. Trends verfolgen & Daten analysieren: Haken Sie nicht einfach Kästchen an; analysieren Sie die Daten! Identifizieren Sie wiederkehrende Probleme, verfolgen Sie Leistungsindikatoren und nutzen Sie diese Informationen, um Prozessverbesserungen voranzutreiben und Ihr GLP-Programm zu verfeinern. Ein statisches Dokument wird zu einem dynamischen Werkzeug für eine kontinuierliche Qualitätsverbesserung.
Ressourcen & Links
- U.S. Food and Drug Administration (FDA) : The FDA is the primary regulatory body overseeing GLP compliance in the US. Their website provides regulations, guidance documents, and information related to GLP.
- U.S. Environmental Protection Agency (EPA) : The EPA also regulates GLP, particularly related to environmental testing. Their site offers relevant guidance and resources.
- Organisation for Economic Co-operation and Development (OECD) : The OECD provides internationally harmonized GLP principles. This is a key resource for understanding the global perspective on GLP.
- United States Pharmacopeia (USP) : USP provides standards and resources related to quality assurance and control, which are highly relevant to GLP implementation. While not solely focused on GLP, their materials offer valuable insights.
- Pharmaceutical and Medical Devices Agency (PMDA) - Japan : Provides information and guidelines related to GLP as implemented in Japan. Offers a different regional perspective on GLP regulations.
- International Organization for Standardization (ISO) : ISO provides standards and guidelines applicable to quality management systems, many of which align with GLP principles. ISO 9001, in particular, is relevant.
- ASTM International : ASTM develops and publishes voluntary consensus standards used globally. While not exclusively GLP focused, their standards often cover aspects like equipment calibration and validation, which are crucial for GLP compliance.
- NiceQuest : Provides GLP training courses and resources. A commercial offering, but often provides a good overview of GLP principles and requirements.
- ComplianceBridge : Offers GLP consulting, training, and software solutions. Provides practical guidance and support for GLP implementation.
- Global GMP : A resource offering news, regulatory updates, and training related to GMP and GLP. Provides a broad perspective on compliance.
- QSA, Inc. : Provides GLP audits and consulting services. They offer valuable insights into common GLP deficiencies and best practices.
- EMC2 Group : Consulting firm specializing in regulatory compliance, including GLP. Offers training and auditing services.
- SPS Compliance : Provides GLP consulting, auditing, and training services. Focused on helping companies achieve and maintain GLP compliance.
Häufig gestellte Fragen
Wofür steht GLP und warum ist es wichtig?
GLP steht für Good Laboratory Practice (oder: Gute Laborpraxis). Es handelt sich um ein Qualitätsmanagementsystem, das die Zuverlässigkeit und Integrität von nicht-klinischen Laborstudien gewährleisten soll, insbesondere solcher, die für behördliche Anträge (z. B. für Arzneimittel oder Pestizide) vorgelegt werden. Die Einhaltung der GLP-Prinzipien stellt sicher, dass Daten korrekt, nachvollziehbar und vertrauenswürdig sind.
Wer sollte eine GLP-Checkliste verwenden?
Alle Personen, die an der Durchführung oder Leitung von nicht-klinischen Laborstudien beteiligt sind, die die Einhaltung der GLP-Bestimmungen erfordern. Dazu gehören Laborleiter, Prüfstandleiter, Prüfstandpersonal, Datenmanager und Qualitätssicherungspersonal.
Was ist in Ihrer GLP-Checklistenvorlage enthalten?
Unsere Vorlage deckt wesentliche Bereiche der GLP-Konformität ab, darunter die Instandhaltung von Einrichtungen und Geräten, Standardarbeitsanweisungen (SOPs), Personaltraining, Datenmanagement, Studienablauf und Qualitätssicherungsmaßnahmen. Sie ist darauf ausgelegt, an verschiedene Studienarten und organisatorische Anforderungen anpassbar zu sein.
Ist diese Checklisten-Vorlage anpassbar?
Ja! Die Vorlage ist als Ausgangspunkt gedacht. Sie können problemlos Elemente hinzufügen, entfernen oder ändern, um sie an Ihre spezifischen Studienprotokolle, SOPs und regulatorischen Anforderungen anzupassen. Wir ermutigen Benutzer, sie an ihre Bedürfnisse anzupassen.
In welchem Dateiformat ist die Checklistenvorlage verfügbar?
Die Checklisten-Vorlage wird im Microsoft Excel-Format (.xlsx) bereitgestellt, was eine einfache Bearbeitung, Nachverfolgung und Dateneingabe ermöglicht.
Wie nutze ich die Checklisten-Vorlage effektiv?
1. Überprüfen Sie die Elemente der Checkliste und verstehen Sie die zugrunde liegenden GLP-Prinzipien. 2. Passen Sie die Checkliste an Ihre spezifischen Studienprotokolle und SOPs an. 3. Nutzen Sie diese während der Studienplanung, -durchführung und -abschluss. 4. Dokumentieren Sie alle durchgeführten Maßnahmen und jegliche Abweichungen von der Checkliste. 5. Überprüfen und aktualisieren Sie die Checkliste regelmäßig, um ihre fortgesetzte Wirksamkeit sicherzustellen.
Welche Rolle spielt ein Study Director in Bezug auf die GLP-Checkliste?
Der Studienleiter trägt letztendlich die Verantwortung für die Einhaltung der GLP-Richtlinien. Er/Sie sollte aktiv an der Checklistenprozedur teilnehmen, die ausgefüllten Checklisten prüfen und festgestellte Mängel beheben. Die Checkliste dient dem Studienleiter als wertvolles Werkzeug zur Überwachung der Compliance und zur Wahrung der Datenintegrität.
Was passiert, wenn ich bei der Überprüfung eine Abweichung feststelle?
Festgestellte Mängel sind zu dokumentieren, zu untersuchen und zu beheben. Ein Maßnahmenplan zur Behebung der Mängel sollte erstellt und umgesetzt werden, um ein erneutes Auftreten zu verhindern. Die Checklisten-Dokumentation sollte den Mangel, die ergriffenen Maßnahmen und die Wirksamkeitsprüfung klar darlegen.
Kann diese Checkliste auch für Studien verwendet werden, die nicht direkt mit regulatorischen Einreichungen zusammenhängen?
Obwohl die Checkliste unter Berücksichtigung der regulatorischen Anforderungen konzipiert wurde, kann sie an Studien in jedem Labor angepasst werden, in denen eine robuste Datenqualität und Rückverfolgbarkeit unerlässlich sind, auch wenn sie nicht direkt den Aufsichtsbehörden vorgelegt werden.
War dieser Artikel hilfreich?
Demo der Fertigungsmanagementlösung
Hören Sie auf, sich mit Papierkram herumzuschlagen und mit inkompatiblen Systemen zu kämpfen! Unsere Lösung bringt Klarheit und Kontrolle in Ihren Produktionsprozess. Von Standardarbeitsanweisungen (SOPs) und Geräteinstandhaltung bis hin zur Qualitätskontrolle und Bestandsverfolgung vereinfachen wir jeden Schritt.
Verwandte Artikel
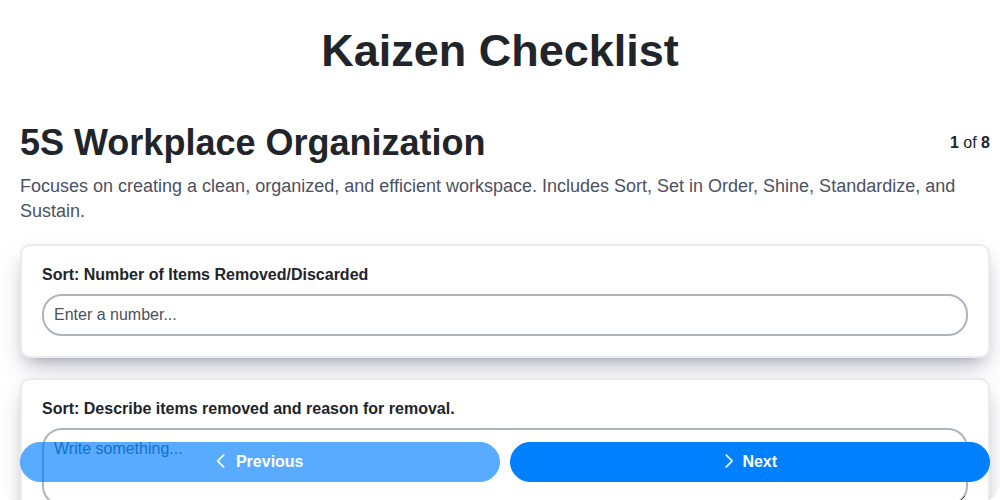
Kaizen-Checklisten-Vorlage: Ihr Weg zur kontinuierlichen Verbesserung

Machine Safety Audit Checklist: Your Guide to a Safer Manufacturing Workplace
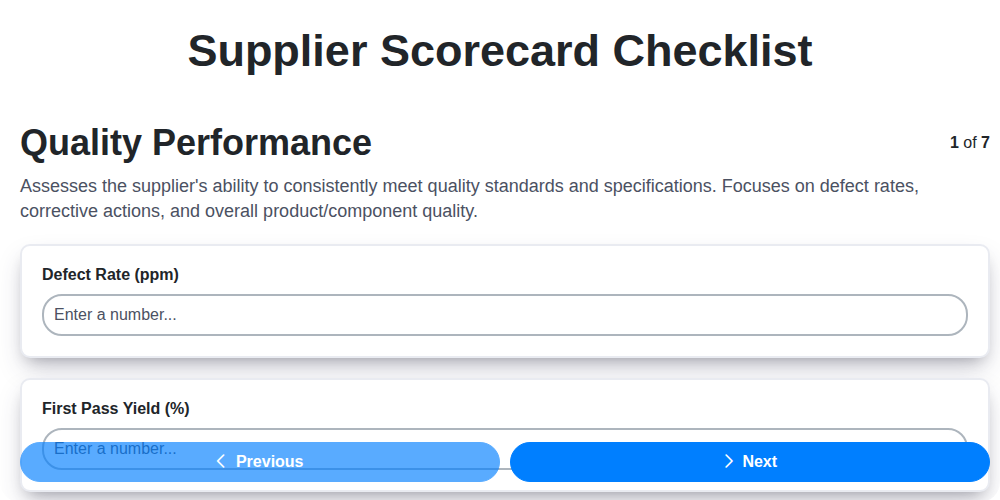
Mastering Supplier Performance: Your Free Supplier Scorecard Checklist Template
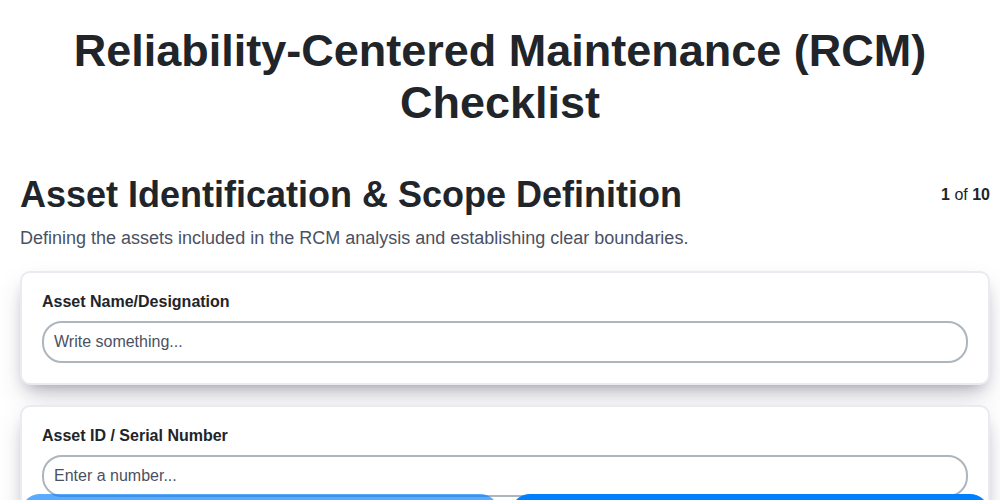
Ihr ultimatives RCM-Checklisten-Template: Ein Schritt-für-Schritt-Leitfaden

LPA-Checklisten-Vorlage: Ihr Leitfaden für mehrschichtige Prozessprüfungen

Ihre ultimative Checklisten-Vorlage für Abschaltung und Kennzeichnung (LOTO)

Your Ultimate FSC 22000 Checklist Template
Qualitätskontroll-Prüflisten-Vorlage: Fehler vermeiden & Fertigungsprozesse verbessern
Gemeinsam schaffen wir das
Benötigen Sie Hilfe bei Checklisten?
Haben Sie eine Frage? Wir helfen Ihnen gerne. Bitte senden Sie uns Ihre Anfrage, und wir werden Ihnen umgehend antworten.