Ihre unverzichtbare GMP-Checklisten-Vorlage: Eine Schritt-für-Schritt-Anleitung
Veröffentlicht: 09/02/2025 Aktualisiert: 04/10/2026
Inhaltsverzeichnis
- Das Fundament verstehen: Was ist eine GMP-Checkliste? (Und warum Sie eine benötigen)
- Ihren Umfang festlegen - Die Checkliste an Ihre Abläufe anpassen
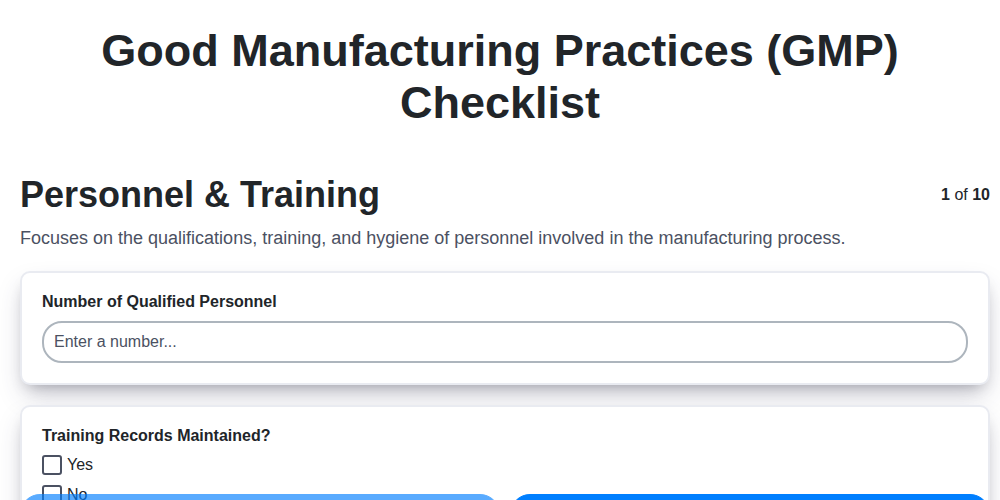
- Personal und Schulung - Aufbau eines qualifizierten Teams
- Einrichtung und Ausrüstung - Aufrechterhaltung einer kontrollierten Umgebung
- Dokumentation und Aufzeichnungen - Gewährleistung der Rückverfolgbarkeit
- Rohstoffe & Komponenten - Qualität von Anfang an
- Fertigungsprozesskontrollen - Konsistente Ausführung
- Abweichungsmanagement & CAPA - Lernen aus Fehlern
- Änderungsmanagement - Effektive Steuerung von Änderungen
- Die Umsetzung Ihrer Checkliste: Implementierung und Überprüfung
- Ressourcen & Links
Kurz gesagt: Erhalten Sie eine kostenlose, anpassbare GMP-Checklistenvorlage, um sicherzustellen, dass Ihre Herstellungsprozesse die Qualitätsstandards erfüllen. Diese Anleitung führt Sie durch den Inhalt der einzelnen Abschnitte - von der Personalschulung bis zur Änderungskontrolle - sodass Sie sie problemlos an Ihre spezifische Branche anpassen und konform bleiben können!
Das Fundament verstehen: Was ist eine GMP-Checkliste? (Und warum Sie eine benötigen)
Eine GMP-Checkliste ist nicht nur ein Dokument; sie ist die praktische Verkörperung Ihres Engagements für Qualität und die Einhaltung gesetzlicher Bestimmungen. Betrachten Sie sie als einen strukturierten, schrittweisen Leitfaden, der sicherstellt, dass jeder kritische Prozess in Ihrem Produktionsbetrieb stets gemäß etablierter Verfahren und regulatorischer Richtlinien durchgeführt wird.
Im Kern beschreibt eine GMP-Checkliste die spezifischen Maßnahmen, Verifizierungen und Aufzeichnungen, die in jeder Phase Ihres Herstellungsprozesses erforderlich sind - vom Wareneingang bis zur Freigabe fertiger Produkte. Diese Punkte sind nicht willkürlich; sie werden sorgfältig ausgewählt, um potenzielle Risiken zu adressieren und die Produkt-Sicherheit, Wirksamkeit und Konsistenz zu gewährleisten.
Warum ist das so wichtig? Weil GMP-Richtlinien, obwohl umfassend, überwältigend sein können. Eine Checkliste verwandelt diese oft komplexen Anforderungen in umsetzbare Schritte, minimiert die Wahrscheinlichkeit menschlicher Fehler, fördert die Rückverfolgbarkeit und liefert konkrete Beweise für die Einhaltung bewährter Verfahren. Es geht um mehr als nur das Abhaken; es ist eine proaktive Maßnahme, die eine Kultur der Qualität in Ihrem gesamten Unternehmen fördert.
Ihren Umfang festlegen - Die Checkliste an Ihre Abläufe anpassen
Eine allgemeine GMP-Checkliste ist zwar ein guter Ausgangspunkt, reicht aber selten für sich allein aus. Die wahre Stärke liegt in der Anpassung - in der genauen Ausrichtung auf Ihre spezifischen Abläufe und behördlichen Auflagen. Bevor Sie mit dem Abhaken beginnen, sollten Sie sich eine gründliche Übersicht über Ihre Prozesse verschaffen.
Beginnen Sie damit, jeden Schritt Ihres Herstellungsprozesses detailliert zu planen - von der Rohstoffannahme bis zur Auslieferung des fertigen Produkts. Identifizieren Sie die kritischen Kontrollpunkte (KKP) innerhalb jedes Schritts; dies sind Punkte, an denen Abweichungen die Produktqualität und -sicherheit erheblich beeinträchtigen könnten. Unterschätzen Sie auch scheinbar unbedeutende Prozesse nicht - selbst administrative Aufgaben können entscheidend sein.
Berücksichtigen Sie das regulatorische Umfeld. Welche GMP-Richtlinien sind für Ihre Branche und die von Ihnen hergestellten Produkte anwendbar? (z. B. 21 CFR Teil 210 & 211 für US-amerikanische Pharmazeutika, EU-GMP-Richtlinien, BRCGS für Lebensmittel). Diese Vorschriften legen spezifische Anforderungen fest, die in Ihrer Prüfliste berücksichtigt werden müssen.
Denken Sie abschließend über die spezifischen Merkmale Ihres Unternehmens nach - die verwendeten Geräte, den Umfang Ihrer Tätigkeiten und alle spezifischen Risiken, die mit Ihren Prozessen verbunden sind. Ihre Checkliste sollte diese Elemente widerspiegeln, um einen wirklich effektiven und relevanten Leitfaden für die Einhaltung der GMP-Richtlinien zu erstellen. Diese anfängliche Bestandsaufnahme legt den Grundstein für eine robuste und auf Ihre Bedürfnisse zugeschnittene GMP-Checkliste, die Ihr Unternehmen und Ihre Kunden wirksam schützt.
Personal und Schulung - Aufbau eines qualifizierten Teams
Ein robustes GMP-System beginnt mit einer gut ausgebildeten und kompetenten Belegschaft. Das Personal bildet das Rückgrat jeder Produktionsanlage, und sein Verständnis für GMP-Prinzipien hat direkten Einfluss auf die Produktqualität und die Sicherheit von Patienten/Verbrauchern. Es reicht nicht aus, einfach nur Mitarbeiter einzustellen; eine kontinuierliche Schulung und die Überprüfung ihres Wissensstandes sind entscheidend.
Wichtige Prüfpunkt-Elemente & Überlegungen:
- Erstausbildung: Alle an der Herstellung, Verarbeitung, Verpackung, Etikettierung und Qualitätskontrolle beteiligten Mitarbeiter sollten eine umfassende Erstausbildung erhalten, die die Grundlagen der GMP, relevante SOPs und Hygienepraktiken abdeckt. Dies sollte praktische Demonstrationen und Bewertungen beinhalten.
- Aufgabenbezogene Schulung: Über das allgemeine GMP-Bewusstsein hinaus muss die Schulung auf spezifische Arbeitsaufgaben und Verantwortlichkeiten zugeschnitten sein. Ein Qualitätskontrollanalyst benötigt andere Kenntnisse als ein Produktionsmitarbeiter.
- Dokumentation hat höchste Priorität.Führen Sie sorgfältige Aufzeichnungen über alle Schulungen, einschließlich Daten, behandelten Themen, Bewertungsergebnissen und Personalunterschriften. Diese Aufzeichnungen dienen als Nachweis der Konformität und können bei Audits entscheidend sein.
- Kompetenzbewertung: Nicht nurliefernAusbildungüberprüfenVerständnis. Implementieren Sie regelmäßige Kompetenzbeurteilungen (schriftliche Prüfungen, praktische Demonstrationen, Beobachtungen), um sicherzustellen, dass das Personal sein Wissen effektiv anwenden kann.
- Auffrischungskurse: GMP entwickelt sich ständig weiter, und Prozesse ändern sich. Geplante Auffrischungsschulungen halten die Mitarbeiter über neue Vorschriften, Verfahren und Best Practices auf dem Laufenden. Die Häufigkeit richtet sich nach der jeweiligen Position und den sich ändernden Anforderungen.
- Hygiene & Persönliche Praktiken: Verstärken Sie die Bedeutung persönlicher Hygiene und sicherer Arbeitsweisen. Dazu gehören das Händewaschen, die korrekte Verwendung persönlicher Schutzausrüstung (PSA) und die Meldung gesundheitlicher Bedenken, die die Produktqualität beeinträchtigen könnten.
- Auftragsnehmer-Schulung: Vergessen Sie nicht Auftragnehmer oder befristet Angestellte! Sie müssen eine angemessene GMP-Schulung erhalten, die für ihre zugewiesenen Aufgaben relevant ist und oft der Schulung entspricht, die Dauerbeschäftigten erhalten.
- Aufbewahrung von Aufzeichnungen: Legen Sie klare Verfahren für die Aufbewahrung von Ausbildungsunterlagen für den erforderlichen Zeitraum fest, wie von den regulatorischen Richtlinien vorgegeben.
Ein gut ausgebildetes Team ist Ihre erste Verteidigungslinie gegen Qualitätsprobleme - investieren Sie in ihre Weiterentwicklung und stellen Sie sicher, dass sie das Wissen und die Fähigkeiten besitzen, um sicher und wirksame Produkte konsequent herzustellen.
Einrichtung und Ausrüstung - Aufrechterhaltung einer kontrollierten Umgebung
Ein robustes GMP-System beruht auf der Integrität Ihrer Einrichtung und der Zuverlässigkeit Ihrer Geräte. Das geht weit über eine bloß saubere Umgebung hinaus; es geht darum, eine kontrollierte Umgebung zu schaffen und aufrechtzuerhalten, die das Risiko von Kontamination, Kreuzkontamination und Fehlern minimiert.
Einrichtungsaspekte:
Die Gestaltung und Anordnung Ihrer Anlage spielen eine entscheidende Rolle. Bitte beachten Sie die folgenden wesentlichen Punkte:
- Kontrollierter Zugang: Beschränken Sie den Zugang zu Produktionsbereichen auf befugtes Personal. Implementieren Sie umfassende Sicherheitsmaßnahmen und Besucherprotokolle.
- Richtige Belüftung und Luftbehandlung: Sorgen Sie für eine ausreichende Belüftung und Luftfiltersysteme, um luftgetragene Schadstoffe zu minimieren. Überwachen und warten Sie diese Systeme regelmäßig, einschließlich HEPA-Filter, sofern zutreffend.
- Trennung von Aktivitäten: Definieren und trennen Sie verschiedene Bereiche klar nach Risikograd, beispielsweise die Lagerung von Rohstoffen, die Verarbeitung, die Verpackung und die Quarantäne. Verhindern Sie eine Kreuzkontamination zwischen diesen Bereichen.
- Schädlingsbekämpfung: Implementieren Sie ein umfassendes Schädlingsbekämpfungsprogramm, um Befälle zu verhindern. Dies beinhaltet regelmäßige Inspektionen, Fallenstellerei und vorbeugende Maßnahmen. Dokumentieren Sie alle Tätigkeiten sorgfältig.
- Oberflächenmaterialien: Verwenden Sie Materialien, die strapazierfähig, nicht fusselnd, leicht zu reinigen und beständig gegen in Ihren Prozessen verwendete Chemikalien sind. Vermeiden Sie nach Möglichkeit poröse Materialien.
- Beleuchtung: Ausreichende und angemessene Beleuchtung ist entscheidend für die Sicht und die Sicherheit der Bediener.
Anlagensicherheit
Die Qualität Ihrer Ausrüstung ist nur so gut wie ihre Wartung. Eine proaktive Herangehensweise an das Geräte-Management ist unerlässlich.
- Wartungspläne zur VorbeugungErstellen und halten Sie sich strikt an Wartungspläne für alle kritischen Anlagen. Dokumentieren Sie alle Wartungsarbeiten.
- Kalibrierung & Validierung: Kalibrieren und validieren Sie die Ausrüstung regelmäßig, um Genauigkeit und Zuverlässigkeit sicherzustellen. Führen Sie detaillierte Aufzeichnungen über diese Tätigkeiten.
- Gerätekonstruktion & Materialien: Wählen Sie Geräte aus, die aus Materialien bestehen, die mit den Produkten und Reinigungsmitteln kompatibel sind.
- Reinigung & Desinfektion: Entwickeln und validieren Sie robuste Reinigungs- und Desinfektionsverfahren für alle Geräte. Dokumentieren Sie diese Verfahren und überprüfen Sie deren Wirksamkeit.
- Gerätequalifizierung: Stellen Sie sicher, dass alle neuen Geräte vor der Benutzung ordnungsgemäß qualifiziert sind, um zu bestätigen, dass sie wie vorgesehen funktionieren und alle Anforderungen erfüllen. Dies umfasst die Installationsqualifizierung (IQ), die Betriebsqualifizierung (OQ) und die Leistungsqualifizierung (PQ).
- Änderungsmanagement für Anlagen: Änderungen oder Reparaturen an Geräten sollten sorgfältig über ein Änderungsmanagement-System verwaltet werden, um sicherzustellen, dass die Produktqualität oder die Prozessvalidierung nicht beeinträchtigt werden.
Dokumentation und Aufzeichnungen - Gewährleistung der Rückverfolgbarkeit
Eine robuste Dokumentation geht über die reine Abhaken von Punkten hinaus; sie ist das Rückgrat eines konformen und effizienten GMP-Systems. Jeder Schritt, von der Rohstoffannahme bis zur Freigabe des Endprodukts, sollte sorgfältig dokumentiert und jederzeit zugänglich sein. Betrachten Sie Ihre Dokumentation als eine detaillierte Schilderung des Produktwegs - eine Geschichte, die für jeden verständlich sein muss, einschließlich für Auditoren.
Warum ist das so wichtig?Rückverfolgbarkeit. Im Falle eines Rückrufs, einer Untersuchung oder eines Qualitätsproblems ermöglichen vollständige und korrekte Aufzeichnungen, die Ursache des Problems schnell zu identifizieren, die Auswirkungen einzuschätzen und Korrekturmaßnahmen umzusetzen. Ohne diese Transparenz agieren Sie im Blindflug.
Was muss dokumentiert werden?Die Liste ist umfangreich, aber wichtige Bereiche sind:
- Standardarbeitsanweisungen (SOPs)Detaillierte Anweisungen für alle Prozesse, regelmäßig überprüft und genehmigt.
- Chargenprotokolle: Vollständige Aufzeichnungen für jede Produktionscharge, einschließlich der verwendeten Rohstoffe, Maschineneinstellungen, Bedienerschritte und Testergebnisse.
- Geräte-Kalibrierungs- und Wartungsprotokolle: Nachweis der ordnungsgemäßen Funktion und Einhaltung der Spezifikationen.
- Schulungsunterlagen: Dokumentation der Mitarbeiterschulungen, die die Kompetenz in ihren jeweiligen Aufgabenbereichen nachweist.
- Abweichungsberichte: Dokumentation aller Abweichungen von etablierten Verfahren, einschließlich Untersuchungsergebnissen und Korrekturmaßnahmen.
- Änderungsdokumentation: Dokumentation aller Änderungen an Prozessen, Geräten oder Materialien, einschließlich der Auswirkungen und Genehmigungen.
Wesentliche Prinzipien für eine effektive Dokumentation:
- Präzision: Stellen Sie sicher, dass die Daten korrekt, vollständig und lesbar sind.
- Chronologische ReihenfolgeAufzeichnungen sind in chronologischer Reihenfolge zu führen.
- Originalaufzeichnungen: Originalaufzeichnungen (oder beglaubigte Kopien) aufbewahren.
- Kontrollierter Zugang: Beschränken Sie den Zugriff auf Akten auf befugtes Personal.
- Sichere Lagerung: Lagern Sie die Aufzeichnungen in einer sicheren und klimatisierten Umgebung.
- Regelmäßige Überprüfung: Überprüfen Sie die Aufzeichnungen regelmäßig, um Genauigkeit und Vollständigkeit sicherzustellen.
- Elektronische Aufzeichnungen: Bei der Verwendung elektronischer Aufzeichnungen ist sicherzustellen, dass die Systeme validiert und den einschlägigen Vorschriften entsprechen (z. B. 21 CFR Teil 11 für Pharmazeutika in den USA).
Rohstoffe & Komponenten - Qualität von Anfang an
Das Sprichwort, aus einem Schweinsöhrchen könne man keinen Seidenschal machen, trifft auch in der Produktion zu. Die Qualität Ihres Endprodukts steht in untrennbarer Verbindung mit der Qualität der verwendeten Rohmaterialien und Komponenten. Ein solides Rohmaterialmanagement ist nicht nur eine regulatorische Anforderung, sondern ein fundamentales Element eines erfolgreichen Qualitätsmanagementsystems.
Dieser Abschnitt konzentriert sich auf die Einführung von Kontrollen, die sicherstellen, dass nur geeignete Materialien in Ihren Produktionsprozess gelangen. Es geht dabei über die bloße Bestellung bei einem Lieferanten hinaus; es umfasst den gesamten Lebenszyklus einer Komponente, von der ersten Beschaffung bis zur Verwendung.
Wesentliche Elemente eines Programms zur Rohstoff- und Bauteilkontrolle:
- Lieferantenqualifizierung: Wählen Sie einen Lieferanten nicht nur aufgrund des Preises aus. Implementieren Sie einen strengen Qualifizierungsprozess, einschließlich Audits (sowohl angekündigt als auch unangemeldet), Überprüfung der Qualitätssicherungssysteme und Verifikation der Einhaltung relevanter Vorschriften. Dies schafft Vertrauen und Verantwortlichkeit.
- Eingangsinspektion und Prüfung: Jede eingehende Materialcharge sollte einer Inspektion und Prüfung gemäß den festgelegten Spezifikationen unterzogen werden. Dies umfasst visuelle Prüfungen, analytische Tests (z. B. Reinheit, Identität, Potenz) und gegebenenfalls auch eine sensorische Bewertung, abhängig vom Material. Klar definierte Stichprobenpläne sind unerlässlich.
- Materialidentifikation & Rückverfolgbarkeit: Implementieren Sie ein System, das es Ihnen ermöglicht, jede Materialcharge eindeutig zu identifizieren und auf ihren Lieferanten sowie auf die zugehörige Dokumentation zurückzuverfolgen. Eindeutige Chargennummern, Barcode-Scannen und elektronische Verfolgungssysteme sind wertvolle Werkzeuge.
- Quarantäne & Entlassung: Eingehende Materialien müssen bis zur Inspektion, Prüfung und Freigabe zur Verwendung in Quarantäne gehalten werden. Ein klar definiertes Freigabeverfahren, das von autorisiertem Personal dokumentiert wird, verhindert die versehentliche Verwendung nicht konformer Materialien.
- Lagerbedingungen: Die sachgerechte Lagerung ist entscheidend für die Wahrung der Materialbeschaffenheit. Beachten Sie bei der Kontrolle von Temperatur, Luftfeuchtigkeit, Lichteinwirkung und anderen Umwelteinflüssen die Angaben im Datenblatt des Materials.
- Materialstatus & Haltbarkeit: Verfolgen Sie den Materialstatus (z. B. unter Quarantäne, genehmigt, abgelaufen) und verwalten Sie die Haltbarkeit sorgfältig. Die FIFO-Prinzipien (First-In, First-Out) sind strikt einzuhalten.
- Nichtkonformitätsmanagement: Legen Sie ein klares Verfahren für den Umgang mit nicht konformen Materialien fest, einschließlich Dokumentation, Untersuchung und Trennung. Abgelehntes Material ist an den Lieferanten zurückzugeben oder ordnungsgemäß zu entsorgen.
Durch die Umsetzung dieser Maßnahmen schaffen Sie eine solide Grundlage für Qualität und minimieren das Risiko von Produktfehlern, die auf minderwertigen Rohstoffen beruhen.
Fertigungsprozesskontrollen - Konsistente Ausführung
Prozesskontrollen in der Fertigung sind das Rückgrat der Qualitätsproduktion. Es reicht nicht aus, umhabenvalidierte Prozesse; Sie müssen diese konsequent ausführen. Das bedeutet, sicherzustellen, dass jede Charge, jeder Schritt gemäß den festgelegten Verfahren durchgeführt wird und jegliche Abweichungen umgehend identifiziert und behoben werden.
Betrachten Sie es wie ein Rezept - selbst das beste Rezept ist nutzlos, wenn die Zutaten nicht korrekt abgemessen oder die Kochzeit nicht stimmt. Ebenso sind robuste SOPs (Standard Operating Procedures) nur dann wirksam, wenn sie gewissenhaft befolgt werden.
Schlüsselkomponenten für eine konsistente Umsetzung:
- Prozessbegleitende Prüfung: Überwachen Sie regelmäßig kritische Parameter (Temperatur, pH-Wert, Viskosität usw.) während des gesamten Herstellungsprozesses. Implementieren Sie einen klaren Zeitplan für Tests und stellen Sie sicher, dass die Ergebnisse genau erfasst und bewertet werden.
- Chargenprotokolle: Dies sind die detaillierten Protokolle Ihres Herstellungsprozesses. Sie sollten dokumentieren.alles- von Rohmaterial-Losnummern bis hin zu Geräteinstellungen und Initialen der Bediener. Genaue und vollständige Chargenprotokolle sind unerlässlich für Rückverfolgbarkeit und Ermittlungen.
- Betriebsausbildung und Kompetenz: Mitarbeiter, die Fertigungsschritte ausführen, müssen angemessen geschult und in der Lage sein, diese Aufgaben kompetent auszuführen. Dies ist kein einmaliges Ereignis; fortlaufende Schulungen und Auffrischungskurse sind entscheidend.
- Gerätekalibrierung & Wartung: Ordnungsgemäß kalibrierte und gewartete Anlagen sorgen für zuverlässige und reproduzierbare Ergebnisse und minimieren die Variabilität in Ihrem Prozess.
- Abweichungsmanagement: Abweichungen von etablierten Verfahren müssen umgehend dokumentiert, untersucht und behoben werden. Dies hilft, potenzielle Probleme zu identifizieren und ein erneutes Auftreten zu verhindern.
- Echtzeitüberwachung (sofern zutreffend): Die Implementierung von Echtzeit-Überwachungssystemen kann sofortige Warnungen bei Abweichungen liefern und ermöglicht proaktive Korrekturmaßnahmen. Dies ist besonders wertvoll für hochsensible Prozesse.
Konsistenz bedeutet nicht nur, Regeln zu befolgen, sondern Qualität in jeden Aspekt Ihres Produktionsprozesses zu integrieren.
Abweichungsmanagement & CAPA - Lernen aus Fehlern
Abweichungen - also die ungeplanten Abweichungen von etablierten Verfahren - sind in jedem Fertigungsprozess unvermeidlich. Das Ziel ist nicht, sie vollständig auszuschalten (ein unrealistisches Ziel!), sondern ein robustes System zur Identifizierung, Untersuchung und Behebung zu etablieren. Hier kommen das Abweichenmanagement und die Maßnahmen zur Korrektur und Vorbeugung (CAPA) ins Spiel. Stellen Sie es sich als einen Lernkreislauf vor: Ein Fehler tritt auf, Sie verstehen, warum er aufgetreten ist, Sie beheben ihn und verhindern, dass er erneut auftritt.
Ein gut strukturiertes Abweichungsmanagement umfasst klare Meldeverfahren, die sicherstellen, dass jede Abweichung - unabhängig davon, wie geringfügig sie scheinen mag - sofort dokumentiert wird. Diese Dokumentation sollte Details wie Datum, Uhrzeit, Beschreibung der Abweichung, beteiligte Personen und die unmittelbar ergriffene Korrekturmaßnahme erfassen. Unterschätzen Sie geringfügige Abweichungen nicht; sie können frühe Warnsignale für größere systemische Probleme sein.
Die Untersuchungsphase ist entscheidend. Sie erfordert eine umfassende Ursachenanalyse, um festzustellenwarumDie Abweichung trat auf. Es reicht nicht, nur das Symptom zu beheben; Sie müssen die zugrunde liegende Ursache verstehen. War es ein Schulungsproblem, ein defektes Gerät, eine Verfahrenslücke oder etwas ganz anderes? Die Anwendung von Techniken wie der 5-Warum-Methode kann dabei sehr hilfreich sein, um tiefergehende Ursachen zu identifizieren.
Sobald die Ursache ermittelt ist, zielt die korrigierende Maßnahme darauf ab, genau dieses Problem zu beheben. Präventive Maßnahmen hingegen sind proaktive Schritte, die dazu dienen, zukünftig ähnliche Abweichungen zu verhindern. Beide Arten von Maßnahmen müssen klar dokumentiert, umgesetzt und verfolgt werden.
Es ist entscheidend, die Wirksamkeit von korrigierenden und präventiven Maßnahmen zu überprüfen. Haben die Maßnahmen das Problem tatsächlich gelöst und ein erneutes Auftreten verhindert? Eine regelmäßige Überprüfung der Abweichungsdaten und der Wirksamkeit von Korrekturmaßnahmen und Vorbeugungsmaßnahmen (CAPA) ist für die kontinuierliche Verbesserung Ihres Qualitätsmanagementsystems unerlässlich. Ein robustes CAPA-System wandelt Abweichungen von potenziellen Rückschlägen in wertvolle Möglichkeiten zum Lernen und zur Weiterentwicklung um.
Änderungsmanagement - Effektive Steuerung von Änderungen
Veränderungen sind in jeder Produktionsumgebung unvermeidlich. Ob es sich um eine Anpassung eines Prozesses, ein Upgrade der Ausrüstung oder eine Modifikation der Rohstoffe handelt, können Änderungen die Produktqualität und Sicherheit beeinträchtigen. Hier wird ein robustes Änderungsmanagementverfahren unerlässlich. Es geht nicht nur darum, Änderungen vorzunehmen, sondern darum, sie zu verwalten.effektivum Risiken zu minimieren und die Einhaltung sicherzustellen.
Ein klar definierter Änderungskontrollprozess stellt sicher, dass jede vorgeschlagene Änderung vor der Umsetzung einer gründlichen Bewertung unterzogen wird. Diese Bewertung sollte die potenziellen Auswirkungen auf Produktqualität, Prozessvalidierung, Gerätequalifizierung und Dokumentation berücksichtigen. Es handelt sich um einen vielschichtigen Ansatz, der die Beiträge verschiedener Abteilungen - Fertigung, Qualitätssicherung, Entwicklung und gegebenenfalls weitere - beinhaltet, um einen ganzheitlichen Überblick über die Änderung zu gewährleisten.
Wesentliche Elemente eines robusten Change-Management-Systems umfassen:
- Änderungsanfrageinitiierung: Ein förmliches Verfahren zur Einreichung geplanter Änderungen, das die Begründung, den Umfang und die voraussichtlichen Auswirkungen klar darlegt.
- Auswirkungsanalyse: Eine detaillierte Analyse, wie sich die Änderung verschiedene Aspekte des Herstellungsprozesses beeinflussen wird, einschließlich Qualität, Sicherheit und Einhaltung gesetzlicher Bestimmungen.
- Risikobewertung: Die potenziellen Risiken im Zusammenhang mit der Veränderung zu identifizieren und zu bewerten sowie Minderungsstrategien zu entwickeln.
- Genehmigungsworkflow: Ein dokumentierter Prozess zur Überprüfung und Genehmigung von Änderungen, der benannte Personen mit der Autorität und dem Fachwissen zur fundierten Entscheidungsfindung beinhaltet.
- Implementierung & Validierung: Sorgfältige Durchführung der Änderung, gefolgt von Validierung oder erneuter Validierung, um sicherzustellen, dass die Produktqualität nicht beeinträchtigt wird.
- Dokumentation und Unterlagenverwaltung: Eine detaillierte Dokumentation des Änderungsprozesses, einschließlich der ursprünglichen Anfrage, der Folgenabschätzung, der Risikobewertung, der Genehmigungsdokumentation und der Validierungsergebnisse.
Das Versäumnis, ein robustes Änderungskontrollsystem zu implementieren, kann zu kostspieligen Fehlern, Rückrufen von Produkten, behördlicher Kontrolle und einem Imageschaden für Ihr Unternehmen führen. Es ist eine vorausschauende Investition in die Wahrung der Integrität Ihrer Produktionsabläufe und demonstriert Ihr Engagement für Qualität und Compliance.
Die Umsetzung Ihrer Checkliste: Implementierung und Überprüfung
Die Erstellung einer GMP-Checkliste ist nur die halbe Miete. Der eigentliche Wert liegt in der konsequentenverwendenund sicherzustellen, dass es weiterhin wirksam bleibt. Hier erfahren Sie, wie Sie Ihre Checkliste erfolgreich in Ihre täglichen Abläufe integrieren und mit sich ändernden Anforderungen in Einklang halten können.
Verantwortung und Schulung zuweisen: Lassen Sie Ihre Checkliste nicht zu einem staubigen Dokument werden. Weisen Sie jeder Checklistenposition klare Verantwortlichkeiten zu. Einzelpersonen oder Teams sollten für die Durchführung der Prüfungen, die Dokumentation der Ergebnisse und die Eskalation von Problemen verantwortlich sein. Entscheidend ist, dass Sie eine umfassende Schulung darüber geben, wie jede Checklistenposition korrekt ausgeführt wird und die zugrunde liegenden GMP-Prinzipien verstanden werden. Regelmäßige Auffrischungsschulungen sind unerlässlich.
2. In den Arbeitsablauf integrieren: Die Checkliste sollte keine zusätzliche Belastung darstellen. Integrieren Sie sie nahtlos in bestehende Arbeitsabläufe. Dies kann die Einbindung von Checklistenpunkten in Standardarbeitsanweisungen (SOPs), die Verwendung digitaler Checklisten-Apps oder die Verknüpfung mit Chargenprotokollen beinhalten. Überlegen Sie, wie Sie Unterbrechungen minimieren und gleichzeitig die Effektivität maximieren können.
3. Nutzen Sie digitale Lösungen: Auch wenn Papier-Checklisten ihren Platz haben, bieten digitale Lösungen deutliche Vorteile. Sie können die Datenerfassung automatisieren, Echtzeitberichte ermöglichen, die Datenrichtigkeit verbessern und Prüfspuren vereinfachen. Erforschen Sie Optionen wie tabletbasierte Checklisten, Cloud-basierte Plattformen und elektronische Dokumentenverwaltungssysteme.
4. Regelmäßige Überprüfung und Prüfung: Ihre GMP-Checkliste ist kein statisches Dokument. Planen Sie regelmäßige Überprüfungen - mindestens jährlich und idealerweise häufiger - um ihre anhaltende Relevanz sicherzustellen. Führen Sie interne Audits durch, um die Einhaltung der Checkliste zu überprüfen und Verbesserungspotenziale zu identifizieren. Vergleichen Sie die Ergebnisse mit früheren Zeiträumen, um die Leistung zu verfolgen und Trends zu erkennen.
5. Management-Prüfung & Kontinuierliche Verbesserung: Die Überprüfung der Checklistenleistung durch das Management ist unerlässlich. Dies bietet eine Plattform, um Ergebnisse zu besprechen, Korrekturmaßnahmen zu priorisieren und die Checkliste auf Basis von gewonnenen Erkenntnissen zu aktualisieren. Fördern Sie eine Kultur der kontinuierlichen Verbesserung, in der Feedback aus allen Ebenen der Organisation willkommen geheißen und berücksichtigt wird. Denken Sie daran, dass GMP eine Reise und kein Ziel ist.
Ressourcen & Links
- FDA Biopharmaceutical CGMP Q&A : Official FDA guidance documents and frequently asked questions related to current Good Manufacturing Practices (cGMP) for biopharmaceutical products. A crucial resource for understanding regulatory expectations.
- ISO 211 - Pharmaceutical GxP Auditing : Provides a framework for auditing pharmaceutical quality systems and is frequently referenced when discussing GMP. Useful for understanding auditing standards.
- United States Pharmacopeia (USP) : Provides standards for pharmaceutical ingredients, excipients, and dosage forms. Relevant for ensuring quality and consistency in raw materials and finished products.
- American Society for Quality (ASQ) : A professional organization dedicated to quality. Provides resources, training, and publications related to quality management, including GMP principles.
- Pharmaceutical Online : Industry news, articles, and resources covering pharmaceutical manufacturing, quality, and regulatory compliance. Provides insights into current trends and best practices.
- GMP Compliance : Provides news, resources, and training focused specifically on GMP compliance. Offers practical advice and regulatory updates.
- ComplianceWorld : Offers a range of compliance resources, including articles, webinars, and training materials covering GMP and other regulated industries. Useful for keeping up with regulatory changes.
- EMC2 : Specializes in regulatory compliance software and services, including solutions for managing GMP documentation and training. Useful for understanding technology-driven solutions.
- MasterControl : Offers quality management system (QMS) software that often incorporates GMP compliance features. Provides insights into digital implementation of GMP processes.
- NSF International : Provides certification and testing services related to food, water, and pharmaceutical products. Relevant for ensuring compliance with specific standards and quality requirements.
- Centers for Disease Control and Prevention (CDC) : While broader, the CDC website can provide valuable information on contamination control, hygiene, and sanitation - critical aspects of maintaining a controlled facility environment.
Häufig gestellte Fragen
Wofür steht GMP und warum ist es wichtig?
GMP steht für Good Manufacturing Practices. Es ist ein System zur Sicherstellung, dass Produkte stets gemäß Qualitätsstandards hergestellt und kontrolliert werden. Es ist für Branchen wie Pharma, Lebensmittel und Kosmetik von entscheidender Bedeutung, um die Sicherheit der Verbraucher und die Wirksamkeit der Produkte zu gewährleisten.
Wer sollte eine GMP-Checkliste verwenden?
Jedes Unternehmen, das Produkte herstellt, die von einer Regulierungsbehörde (wie der FDA in den USA) reguliert werden, sollte eine GMP-Checkliste verwenden. Dazu gehören Hersteller, Zulieferer und Distributoren.
Welche Arten von Produkten sind typischerweise durch GMP-Bestimmungen abgedeckt?
GMP-Bestimmungen umfassen häufig Pharmazeutika, biologische Arzneimittel, Medizinprodukte, Lebensmittel, Nahrungsergänzungsmittel, Kosmetika und pharmazeutische Wirkstoffe (API).
Was gehört zu einer typischen GMP-Checklistenvorlage?
Eine umfassende GMP-Checkliste umfasst in der Regel Abschnitte zu Personaltraining, Anlagenvalidierung, Instandhaltung der Räumlichkeiten, Dokumentenlenkung, Qualitätskontrolle, Umgang mit Rohstoffen und Abweichungsmanagement.
Kann ich die in dem Artikel bereitgestellte GMP-Checklisten-Vorlage ändern?
Ja, die Vorlage ist zur Anpassung gedacht. Sie sollten sie an Ihre spezifischen Prozesse, Produkte und regulatorischen Anforderungen anpassen. Überprüfen und aktualisieren Sie Ihre Checkliste regelmäßig, um Änderungen widerzuspiegeln.
Was ist der Unterschied zwischen einer GMP-Checkliste und einer Standardarbeitsanweisung (SOP)?
Eine GMP-Checkliste ist ein Dokument, das verwendet wird, um zu überprüfen, ob SOPs eingehalten werden. SOPs hingegen beschreiben genau *wie* eine bestimmte Aufgabe auszuführen ist. Eine Checkliste bestätigt die Einhaltung der SOPs.
Wie oft sollte eine GMP-Checkliste überprüft und aktualisiert werden?
GMP-Checklisten sollten mindestens jährlich überprüft und aktualisiert werden, oder häufiger, wenn es wesentliche Änderungen in Prozessen, Vorschriften oder Prüfungsergebnissen gibt.
Was geschieht, wenn eine GMP-Prüfung Abweichungen feststellt?
Nichteinhaltungen können zu Verwarnschreiben, Produktzurückrufen, Einfuhrverbote und sogar rechtlichen Schritten führen. Es ist entscheidend, Feststellungen umgehend mit Korrektur- und Präventivmaßnahmen (CAPA) zu beheben.
Wo finde ich weitere Informationen zu den GMP-Richtlinien?
Detaillierte Informationen zu GMP-Bestimmungen finden Sie auf den Webseiten von Aufsichtsbehörden wie der FDA (USA), der EMA (Europa) und anderen, die für Ihre Region und Branche spezifisch sind.
Wie kann ich feststellen, ob meine GMP-Checkliste wirklich wirksam ist?
Eine effektive Checkliste wird regelmäßig verwendet, basierend auf den Ergebnissen von Audits und Änderungen in den Prozessen aktualisiert und zeigt eine konsequente Einhaltung der GMP-Anforderungen. Regelmäßige interne Audits können helfen, ihre Effektivität zu beurteilen.
War dieser Artikel hilfreich?
Demo der Fertigungsmanagementlösung
Hören Sie auf, sich mit Papierkram herumzuschlagen und mit inkompatiblen Systemen zu kämpfen! Unsere Lösung bringt Klarheit und Kontrolle in Ihren Produktionsprozess. Von Standardarbeitsanweisungen (SOPs) und Geräteinstandhaltung bis hin zur Qualitätskontrolle und Bestandsverfolgung vereinfachen wir jeden Schritt.
Verwandte Artikel
Kaizen-Checklisten-Vorlage: Ihr Weg zur kontinuierlichen Verbesserung

Machine Safety Audit Checklist: Your Guide to a Safer Manufacturing Workplace
Mastering Supplier Performance: Your Free Supplier Scorecard Checklist Template
Ihr ultimatives RCM-Checklisten-Template: Ein Schritt-für-Schritt-Leitfaden

LPA-Checklisten-Vorlage: Ihr Leitfaden für mehrschichtige Prozessprüfungen

Ihre ultimative Checklisten-Vorlage für Abschaltung und Kennzeichnung (LOTO)

Your Ultimate FSC 22000 Checklist Template
Qualitätskontroll-Prüflisten-Vorlage: Fehler vermeiden & Fertigungsprozesse verbessern
Gemeinsam schaffen wir das
Benötigen Sie Hilfe bei Checklisten?
Haben Sie eine Frage? Wir helfen Ihnen gerne. Bitte senden Sie uns Ihre Anfrage, und wir werden Ihnen umgehend antworten.