Tu plantilla esencial de lista de verificación de GLP: Una guía práctica
Publicado: 09/01/2025 Actualizado: 03/19/2026
Índice
- Introducción: Por qué es importante una lista de verificación de GLP
- Comprendiendo los Principios Fundamentales de las BPL
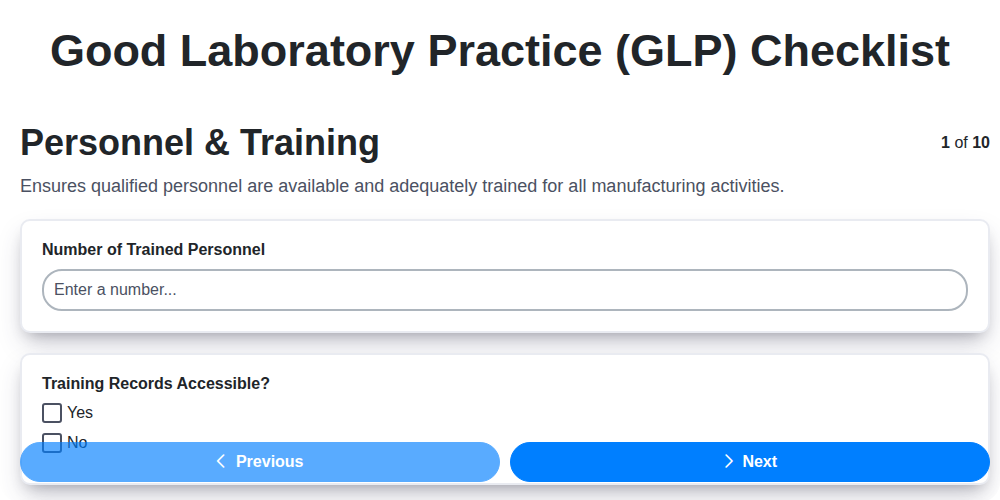
- Sección 1: Personal y Capacitación - Construyendo un Equipo Cualificado
- Sección 2: Instalaciones y Equipos - Garantizando un Entorno Controlado
- Sección 3: Gestión de Materiales - Mantener la Trazabilidad
- Sección 4: Procedimientos operativos estándar (POE) y procedimientos - El fundamento de la coherencia
- Sección 5: Integridad de los Datos y Custodia de Registros: Un Enfoque Crítico
- Sección 6: Control de Calidad y Pruebas - Validación de sus Resultados
- Sección 7: Gestión y Investigación de Desviaciones - Aprendiendo de los Errores
- Sección 8: Control de Cambios: Gestionando Efectivamente las Modificaciones
- Sección 9: Calificación y Validación de Equipos - Demostración de Desempeño
- Sección 10: Validación del Proceso: Asegurando la Reproductibilidad
- Poniendo en práctica tu plantilla de lista de verificación de GLP
- Recursos y Enlaces
TL;DR: ¿Necesita asegurarse de que su laboratorio cumple con las normas de Buena Práctica de Laboratorio (BPL)? Esta guía proporciona una plantilla de lista de verificación práctica que abarca todo, desde la capacitación del personal y el mantenimiento de las instalaciones hasta la gestión y la validación de datos. ¡Descárguela, personalícela para sus procesos y utilícela para realizar un seguimiento sistemático del cumplimiento y mantener la integridad de los datos!
Introducción: Por qué es importante una lista de verificación de GLP
En el mundo de la investigación científica y el desarrollo de productos, la integridad de los datos no es solo un rasgo deseable, sino el fundamento de la credibilidad y el cumplimiento normativo. Las directrices de la Buena Práctica de Laboratorio (BPL) están diseñadas para garantizar que los datos generados sean fiables, trazables y defendibles. Pero saber el...principiosCumplir con GLP es solo la mitad de la batalla. La aplicación constante, la meticulosa llevanza de registros y una vigilancia exhaustiva para el detalle son cruciales para lograr una verdadera conformidad con GLP. Aquí es donde una lista de verificación GLP bien estructurada se convierte en una herramienta invaluable. Más que una simple lista de tareas, una lista de verificación GLP proporciona una hoja de ruta clara para su laboratorio, fomentando una cultura de responsabilidad y minimizando el riesgo de costosos errores o retrocesos regulatorios. Considérela como la garantía de su laboratorio de que cada proceso, cada observación y cada resultado está documentado, validado y, en última instancia, confiable.
Comprendiendo los Principios Fundamentales de las BPL
GLP no es simplemente una lista de reglas; es una filosofía basada en unos pocos pilares fundamentales. En su esencia, reside un compromiso inquebrantable con la integridad de los datos, garantizando que sean precisos, fiables y trazables. Esto va más allá de la mera documentación de observaciones; exige una atención meticulosa al detalle, el cumplimiento de los procedimientos establecidos y un sistema de controles y equilibrios.
Varios principios fundamentales sustentan este compromiso.Planificaciónes primordial. Un protocolo bien definido que describa los objetivos, la metodología y el análisis estadístico del estudio es la base.Rendimientose refiere a la ejecución constante del protocolo por parte de personal capacitado.Documentación es la piedra angular de las BPL - cada acción, observación y cálculo debe registrarse de forma clara y contemporánea.Aseguramiento de la Calidades el organismo independiente que verifica el cumplimiento de las BPL, actuando como una garantía fundamental contra errores y incumplimientos. Finalmente,ArchivoGarantiza la preservación y accesibilidad a largo plazo de los datos para auditorías y futuras referencias. Reconocer y defender estos principios es fundamental para generar datos científicos confiables y lograr una verdadera conformidad con las BPF.
Sección 1: Personal y Capacitación - Construyendo un Equipo Cualificado
El éxito de un laboratorio depende de la pericia y la competencia de su personal. El cumplimiento de las BPL no se trata solo de procedimientos y equipos; fundamentalmente, se trata de contar con un equipo cualificado, dotado del conocimiento y las habilidades necesarias para desempeñar sus funciones con precisión y ética. Esto comienza con una cuidadosa selección y se extiende a la formación continua y la evaluación del desempeño.
Más allá de las credenciales: Evaluación de la competencia
Si bien la educación formal y la experiencia son importantes, una evaluación exhaustiva de las habilidades prácticas es crucial. Los encargados de contratación deberían priorizar a los candidatos que demuestren un sólido conocimiento de los principios GLP y un compromiso con la integridad de los datos. Esta evaluación puede incluir demostraciones prácticas, entrevistas basadas en escenarios y evaluaciones de la capacidad para resolver problemas. Considere evaluaciones basadas en habilidades, alineadas a funciones específicas del puesto.
El Camino del Entrenamiento: Desde la Incorporación hasta la Mejora Continua
La capacitación inicial de incorporación debe cubrir los fundamentos de GLP, los procedimientos operativos estándar (POE) específicos relevantes para el puesto del individuo y los protocolos de seguridad esenciales. Esto debe incluir una revisión de las expectativas de integridad de los datos y la importancia de la llevanza precisa de registros. Registros de capacitación.debese mantendrán meticulosamente, documentando el contenido cubierto, las fechas de capacitación y los nombres de los capacitadores y los participantes.
Desarrollo Continuo - Un Compromiso con el Crecimiento
La capacitación no debe ser un evento aislado. Un programa sólido incorpora cursos de actualización periódicos, información sobre cambios regulatorios y formación sobre nuevas tecnologías o metodologías. Considere la incorporación de oportunidades de capacitación cruzada para ampliar las habilidades del personal y mejorar la flexibilidad. Las evaluaciones de desempeño deben incluir una evaluación del cumplimiento de las BPF (Buenas Prácticas de Fabricación) y la identificación de áreas para el desarrollo profesional. Una cultura de aprendizaje continuo empodera a su equipo para mantener los más altos estándares de calidad y cumplimiento.
Sección 2: Instalaciones y Equipos - Garantizando un Entorno Controlado
La base de datos fiable comienza con un entorno rigurosamente controlado. Las instalaciones y los equipos desempeñan un papel crucial para mantener la integridad de los datos, y un enfoque proactivo en su gestión es primordial. No se trata solo de limpieza; se trata de asegurar condiciones controladas que minimicen la variabilidad y las posibles fuentes de error.
Una sección sólida de Instalaciones y Equipos en su lista de verificación de BPL debe abordar varias áreas clave. Primero, considere la distribución física. ¿Existe espacio suficiente para realizar todos los procedimientos necesarios de manera segura y eficiente? La segregación de materiales incompatibles es vital: prevenir la contaminación accidental es una medida preventiva crítica. Los sistemas de ventilación necesitan inspección y mantenimiento regulares para garantizar una calidad adecuada del aire y la eliminación de humos potencialmente dañinos.
El control de la temperatura y la humedad suele ser esencial, especialmente para muestras o reactivos sensibles. Los programas de monitoreo ambiental documentados, incluyendo el registro y la calibración regulares de los sensores de temperatura y humedad, son fundamentales.
En cuanto al equipamiento, se requiere un enfoque sistemático. Cada equipo utilizado en actividades relacionadas con GLP debe mantenerse y calibrarse correctamente según un programa documentado. Es esencial llevar registros de estas actividades, incluyendo fechas, resultados y personal involucrado. Además del mantenimiento rutinario, se deben realizar y documentar la calificación de instalación (IQ), la calificación operativa (OQ) y la calificación de desempeño (PQ) para el equipamiento crítico, asegurando que esté instalado correctamente, funcione según lo previsto y ofrezca un rendimiento consistente. Finalmente, debe existir un sistema para gestionar el equipamiento no conforme - aquel que está fuera de servicio o requiere reparación - para prevenir su uso no autorizado.
Sección 3: Gestión de Materiales - Mantener la Trazabilidad
Una gestión eficaz de los materiales es la piedra angular del cumplimiento de GLP, impactando directamente la integridad de los datos y su reproducibilidad. No se trata simplemente de almacenar productos químicos, sino de crear una pista de auditoría para cada material utilizado en sus estudios. Esto implica una documentación meticulosa desde el momento en que un material ingresa al laboratorio hasta su eliminación o uso en un producto final.
Elementos clave de la trazabilidad:
- Registros de Inventario Exhaustivos: Un sistema de inventario robusto es primordial. Este debe incluir detalles como la información del proveedor, números de lote, fecha de recepción, fecha de caducidad, cantidad recibida y ubicación dentro del laboratorio. Se recomienda encarecidamente el uso de sistemas digitales para lograr eficiencia y precisión.
- Identificación Única: Cada recipiente de material debe estar identificado de forma única, generalmente mediante etiquetas. Las etiquetas deben incluir el nombre del material, la concentración, el número de lote, la fecha de apertura y las iniciales de la persona que lo abrió.
- Acceso controlado.Limitar el acceso a las áreas de almacenamiento únicamente al personal autorizado. Esto minimiza el riesgo de uso no autorizado o contaminación.
- Muestras retenidas: Conserve muestras representativas de cada lote de material utilizado en los estudios de GLP. Estas muestras deben estar debidamente etiquetadas y almacenadas, y su integridad debe mantenerse. Son vitales para futuras referencias, retests o investigaciones.
- Registros de Uso de Materiales: Mantenga registros detallados documentando el uso de cada material en estudios o experimentos específicos. Estos registros deben incluir la fecha, la cantidad utilizada, el número de estudio y las iniciales de la persona que utiliza el material.
- Auditorías periódicas: Realice auditorías periódicas de su sistema de gestión de materiales para identificar y corregir cualquier discrepancia o debilidad. Esto incluye verificar que los registros sean precisos, los materiales se almacenen correctamente y se monitoreen las fechas de caducidad.
Una gestión eficaz de los materiales no es simplemente un requisito procesal; es una salvaguarda vital que protege la integridad de sus datos y la credibilidad de su investigación.
Sección 4: Procedimientos operativos estándar (POE) y procedimientos - El fundamento de la coherencia
Los Procedimientos Operativos Estándar (POE) no son solo papeleo; son la base de resultados reproducibles y una prueba del compromiso de su laboratorio con la calidad. Considérelos como la memoria colectiva de su laboratorio, documentando...cómoLas tareas se llevan a cabo de forma consistente, cada vez. Sin Procedimientos Operativos Estándar (POE) sólidos, las variaciones se infiltran, los datos se vuelven poco fiables y el cumplimiento se convierte en una lucha constante.
Los Procedimientos Operativos Estándar (POE) eficaces van más allá de simples instrucciones paso a paso. Deben definir claramente el propósito del procedimiento, identificar al personal responsable, especificar los equipos y materiales necesarios, describir las precauciones de seguridad y detallar los resultados esperados. No son documentos estáticos; requieren una revisión y actualización periódicas para reflejar cambios en los procesos, la tecnología o los requisitos reglamentarios.
Es crucial que los Procedimientos Operativos Estándar (POE) sean tan buenos como la capacitación que los acompaña. La verificación de la comprensión, a través de demostraciones prácticas o evaluaciones, es esencial para asegurar que todo el personal siga los procedimientos correctamente. Las auditorías periódicas del cumplimiento de los POE también son vitales para identificar áreas de mejora y reforzar una cultura de cumplimiento. Un programa de POE bien mantenido y utilizado activamente no se trata solo de marcar casillas, sino de construir una base de rigor científico e integridad de datos.
Sección 5: Integridad de los Datos y Custodia de Registros: Un Enfoque Crítico
La integridad de los datos es la piedra angular del cumplimiento de las BPL, y su encarnación práctica es una gestión de registros sólida. No se trata simplemente de documentar lo que ocurrió, sino de garantizar que esos registros sean precisos, completos, coherentes, duraderos y estén disponibles. La integridad de los datos comprometida puede tener graves consecuencias, desde sanciones regulatorias hasta resultados de investigación invalidados.
Esta sección se centra en prácticas esenciales para mantener la integridad de los datos y llevar registros meticulosos:
- Los datos originales son primordiales.Todos los datos brutos generados durante un estudio de GLP - ya sean impresiones de instrumentos, notas manuscritas o registros electrónicos -debeser el registro original. Esto implica que no se debe sobrescribir, eliminar ni alterar ningún dato. Si es necesario realizar correcciones, deben efectuarse mediante una enmienda fechada y con iniciales, que haga referencia clara a la entrada original.
- Registros de auditoría para registros electrónicos: Al utilizar sistemas electrónicos, asegúrese de que los registros de auditoría estén habilitados y funcionen correctamente. Estos registros deben rastrear cada acción realizada dentro del sistema, incluyendo la entrada de datos, modificaciones y eliminaciones. Revise regularmente los registros de auditoría para identificar cualquier anomalía.
- Almacenamiento de datos seguro y control de acceso.Implemente controles de acceso robustos para restringir el acceso a los datos únicamente al personal autorizado. Utilice métodos de almacenamiento seguros (tanto físicos como electrónicos) para proteger los datos contra pérdida, robo o modificación no autorizada.
- Políticas de Retención de Datos: Establezca políticas claras de conservación de datos que cumplan con los requisitos reglamentarios y las directrices organizacionales. Estas políticas deben determinar por cuánto tiempo se deben conservar los registros y cómo se deben archivar.
- Etiquetado y clasificación claros: Asegúrese de que todos los registros estén claramente etiquetados e indexados para facilitar su recuperación y trazabilidad. Esto es especialmente importante para los registros físicos.
- Orden cronológicoMantenga los registros en un orden cronológico estricto para garantizar una representación precisa del avance del estudio.
- Capacitación y concienciación: Capacite regularmente al personal en principios de integridad de datos y mejores prácticas de registro. Fomentar una cultura de conciencia es clave para prevenir errores involuntarios.
Sección 6: Control de Calidad y Pruebas - Validación de sus Resultados
El control de calidad (CC) y las pruebas son pilares fundamentales para obtener datos fiables en cualquier laboratorio que cumpla con las normas de GLP. No es suficiente con simplemente...ejecutar pruebas; debe validar rigurosamente que dichas pruebas sean precisas, exactas y produzcan de forma consistente resultados fiables. Esta sección profundiza en consideraciones clave para procedimientos sólidos de control de calidad y pruebas.
Validación del método: el fundamento de la confianza.
Antes de utilizar cualquier método analítico para estudios relacionados con BPL,debedebe ser validada. La validación demuestra que el método es adecuado para su propósito previsto. Esto suele implicar la evaluación de parámetros como:
- Precisión: Qué cerca esté el resultado de la prueba del valor real.
- Precisión: La repetibilidad y la reproducibilidad de los resultados. (Considerando la repetibilidad - dentro de una misma ejecución, y la reproducibilidad - a través de diferentes analistas, instrumentos y días).
- Especificidad/Selectividad: La capacidad del método para medir únicamente el analito objetivo sin interferencias.
- Límite de Detección (LD): La concentración más baja de analito que puede ser detectada.
- Límite de Cuantificación (LC)La concentración más baja de analito que puede cuantificarse de manera fiable.
- LinealidadEl rango en el que el método proporciona resultados proporcionales.
- RobustezLa capacidad del método para resistir pequeñas variaciones en las condiciones (p. ej., temperatura, pH).
Los estudios de validación se documentan meticulosamente y los criterios de aceptación están claramente definidos.antesComienzan las pruebas. Las desviaciones de estos criterios deben ser investigadas y resueltas antes de que el método pueda considerarse validado.
Control de Calidad Continuo - Más Allá de la Validación Inicial
La validación no es un evento único. El control de calidad (QC) continuo es esencial para mantener la integridad de los datos. Esto incluye:
- Muestras de control: Ejecutar muestras de control con concentraciones conocidas junto con las muestras del estudio para supervisar el rendimiento del sistema analítico. Estas deben ser representativas de la matriz y los analitos que se están analizando.
- Curvas de calibración: Generar y validar regularmente curvas de calibración utilizando estándares de concentraciones conocidas.
- Mantenimiento de Equipos: Implementar un programa de mantenimiento preventivo para todos los equipos analíticos para garantizar su correcto funcionamiento.
- Gestión de Reactivos y Estándares: Control estricto del almacenamiento, manejo y fechas de caducidad de reactivos y patrones de referencia.
- Revisión de datos: Revisión exhaustiva de todos los datos brutos y resultados para identificar cualquier anomalía o tendencia que pueda indicar un problema.
Al priorizar procedimientos rigurosos de control de calidad y pruebas, se construye una base de confianza en sus datos, garantizando el cumplimiento y mejorando la credibilidad de sus resultados de investigación.
Sección 7: Gestión y Investigación de Desviaciones - Aprendiendo de los Errores
Las desviaciones son una parte inevitable de cualquier operación de laboratorio. Representan instancias en las que los procedimientos no se siguieron exactamente como se detallan en los POPs, ocurrieron resultados inesperados o el equipo falló. Sin embargo, la mera existencia de una desviación no es motivo de alarma; es elmanejode esa desviación que realmente importa. Un proceso robusto de gestión de desviaciones no se trata de asignar culpas; se trata de identificar oportunidades de mejora y prevenir la recurrencia.
Un enfoque estructurado para la gestión de desviaciones debe comprender varios pasos clave. Primero,detección y documentaciónSon primordiales. Toda desviación, independientemente de su aparente gravedad, debe registrarse inmediatamente. Esta documentación debe incluir una descripción clara de lo ocurrido, cuándo ocurrió, quiénes estuvieron involucrados y el posible impacto en la integridad de los datos.
A continuación, unainvestigación debe iniciarse. Esto va más allá de simplemente señalar la desviación; requiere profundizar en lacausa raíz¿Fue una deficiencia en la capacitación? ¿Un procedimiento operativo estándar defectuoso? ¿Un fallo de equipo? ¿Un problema sistemático en el proceso? Utilizar herramientas como la técnica de los 5 Porqués puede ser inestimable para descubrir el problema subyacente.
Una vez que se ha identificado la causa raíz, unaacción correctiva y acción preventiva (CAPA) Debe desarrollarse e implementarse un plan. Las acciones correctivas deben abordar el problema inmediato para evitar su repetición en eligualsituación. Las acciones preventivas se dirigen a la causa subyacente para evitar que surjan problemas similares en elotroáreas del laboratorio.
Es crucial que todo el proceso de gestión de desviaciones esté documentado meticulosamente. Esto incluye el informe inicial de la desviación, los hallazgos de la investigación, el plan CAPA y la verificación de que las acciones correctivas y preventivas fueron efectivas. Esta documentación sirve como una valiosa ruta de auditoría y demuestra un compromiso con la mejora continua. Recuerde, una desviación no es un fallo; es una oportunidad de aprendizaje, una posibilidad de fortalecer los procesos de su laboratorio y mejorar la fiabilidad de sus datos.
Sección 8: Control de Cambios: Gestionando Efectivamente las Modificaciones
Los cambios son inevitables en cualquier entorno de laboratorio. Ya sea una actualización de un Procedimiento Operativo Estándar (POE), un nuevo equipo o una modificación a un protocolo de estudio, gestionar estos cambios de manera efectiva es primordial para mantener el cumplimiento de las Buenas Prácticas de Laboratorio (BPL) y la integridad de los datos. Un sistema de control de cambios sólido garantiza que las alteraciones se evalúen, documenten e implementen de manera controlada, minimizando los riesgos potenciales y preservando la fiabilidad de sus datos.
El núcleo de un sistema de control de cambios exitoso gira en torno a un procedimiento documentado. Este procedimiento debe detallar los pasos para iniciar una solicitud de cambio, realizar una evaluación de riesgos para comprender el impacto potencial, obtener las aprobaciones necesarias, implementar el cambio y verificar su efectividad. Es crucial, además, definir quién tiene la autoridad para iniciar, revisar y aprobar los cambios.
No todas las modificaciones ameritan el mismo nivel de escrutinio. Su sistema debe categorizar los cambios en función de su potencial nivel de riesgo - menor, moderado y mayor - y asignar los correspondientes niveles de revisión y requisitos de documentación. Por ejemplo, una corrección tipográfica menor en un Procedimiento Operativo Estándar (POE) podría requerir una simple aprobación y archivo, mientras que una modificación significativa en un proceso de fabricación necesitaría un estudio de validación exhaustivo.
Más allá del cambio inmediato en sí, considere los efectos en cadena. Los cambios en un área a menudo pueden impactar a otras. Su evaluación de riesgos debe identificar proactivamente estos posibles efectos dominó e incluir estrategias de mitigación. La capacitación adecuada también es vital; el personal debe estar informado sobre los cambios y comprender cómo afectan sus funciones y responsabilidades. Finalmente, no olvide revisar periódicamente su procedimiento de control de cambios para garantizar su eficacia y relevancia con respecto a sus operaciones de laboratorio en constante evolución.
Sección 9: Calificación y Validación de Equipos - Demostración de Desempeño
La calificación y validación de equipos no se trata solo de marcar casillas; se trata de proporcionar pruebas demostrables de que su equipo funciona de manera consistente según lo previsto, generando datos fiables. Es un proceso multifacético diseñado para inspirar confianza en cada experimento y resultado.
El proceso de calificación generalmente comprende tres etapas cruciales:
- Calificación de la Instalación (CI)Esto verifica que el equipo se ha instalado correctamente, de acuerdo con las especificaciones del fabricante, y está debidamente conectado a los suministros como electricidad, agua y gas. La documentación incluye números de serie, fechas de instalación e información del proveedor.
- Calificación Operacional (CO): Esta etapa demuestra que el equipo funciona según las especificaciones del fabricante bajo condiciones de operación definidas. Esto a menudo implica pruebas de rendimiento a través de una variedad de parámetros. Los criterios de aceptación están predefinidos y deben cumplirse.
- Calificación de Desempeño (CD): Este es el paso final, confirmando que el equipo funciona de manera consistente según los criterios de aceptación establecidos, cuando se utiliza para su propósito previsto dentro del entorno específico del laboratorio. En esencia, esto valida que el rendimiento del equipo es fiable y reproducible.
La validación se extiende más allá de los equipos. Los métodos analíticos, el software utilizado para la adquisición y el análisis de datos, e incluso los procesos completos, requieren validación para asegurar su exactitud, fiabilidad y adecuación para el cumplimiento de las BPL. Esto implica evidencia documentada de que el método/software/proceso produce consistentemente los resultados esperados cuando se utiliza de acuerdo con los procedimientos predefinidos.
Es crucial mantener la documentación de calificación y validación de manera meticulosa, que sea fácilmente accesible y se revise periódicamente para garantizar el cumplimiento continuo. Cualquier desviación o fallo debe investigarse a fondo y documentarse, implementando y verificando acciones correctivas. El objetivo no es simplemente calificar y validar una vez, sino establecer un sistema para la garantía continua y la mejora continua.
Sección 10: Validación del Proceso: Asegurando la Reproductibilidad
La validación de procesos no es simplemente un complemento deseable; es un pilar fundamental de las BPL y una demostración crítica de su capacidad para producir datos o productos fiables de forma consistente. Va más allá de simplemente seguir un procedimiento: se trata de demostrar que el proceso... siempreFunciona según lo esperado bajo condiciones definidas. Esto implica, típicamente, demostrar que el proceso opera de manera consistente dentro de criterios de aceptación predeterminados.
Existen tres etapas principales de la validación de procesos: Validación del Diseño del Proceso ,Calificación del proceso yVerificación Continua de Procesos (VCP) .
- Validación del Diseño de Procesos: Esta fase se centra en confirmar que el diseño del proceso es robusto y capaz de lograr el resultado deseado. Normalmente, se logra a través de evaluaciones exhaustivas de riesgos, simulaciones y estudios piloto. Esta etapa establece la base de su proceso y su rendimiento esperado.
- Calificación del Proceso: Una vez que el diseño está validado, la cualificación del proceso verifica que éste funcione de manera consistente al ejecutarse bajo condiciones reales de operación. Esto implica ejecutar múltiples ciclos de validación bajo parámetros cuidadosamente controlados, documentando meticulosamente los resultados y demostrando que se cumplen todos los criterios de aceptación.
- Verificación Continua de Procesos (VCP): El CPV es una evaluación continua del proceso validado. Implica el monitoreo periódico de los parámetros críticos del proceso (CPP) y los atributos críticos de la calidad (CQA) para asegurar el control continuo del proceso e identificar cualquier desviación potencial que requiera investigación. Los diagramas de Control Estadístico de Procesos (CEP) se utilizan frecuentemente en el CPV para rastrear tendencias del proceso y activar alertas cuando sea necesario.
La validación de procesos robusta demuestra su compromiso con la integridad de los datos, reduce el riesgo de fallas en los productos y fortalece su posición de cumplimiento normativo. La documentación exhaustiva a lo largo de todo el ciclo de vida de la validación es primordial para la preparación de auditorías y la trazabilidad.
Poniendo en práctica tu plantilla de lista de verificación de GLP
Una lista de verificación estática, por muy exhaustiva que sea, es solo el punto de partida. El cumplimiento real de las BPL exige un enfoque dinámico y proactivo. Así es como puede ir más allá de un documento e integrar activamente su lista de verificación en las operaciones diarias:
Asignar propiedad y responsabilidad.No permitas que tu lista de verificación se cubra de polvo. Asigna a individuos o equipos específicos la responsabilidad de cada sección. Esto asegura que alguien esté monitoreando, actualizando y abordando activamente cualquier problema identificado. Una responsabilidad clara fomenta un sentido de rendición de cuentas y promueve la mejora continua.
Integrar en los flujos de trabajo: Integra sin problemas los elementos de la lista de verificación en los flujos de trabajo existentes del laboratorio. No lo trate como un complemento adicional; incorpórelo como una parte integral de la ejecución de las tareas. Por ejemplo, incluya pasos de verificación de la lista de verificación dentro de los procedimientos operativos estándar (POE) o utilice listas de verificación digitales integradas con los sistemas de gestión de información de laboratorio (SGIL).
Implementar ciclos de revisión periódicos: Establezca ciclos de revisión periódicos (semanales, mensuales, trimestrales) para evaluar sistemáticamente el cumplimiento de la lista de verificación. Estas revisiones no deben ser punitivas; son oportunidades para aprender, identificar cuellos de botella en el proceso y fortalecer las prácticas de GLP.
Aprovechar las herramientas digitales: ¡Aproveche la tecnología! Las plantillas de listas de verificación digitales, integradas con análisis de datos, pueden automatizar recordatorios, rastrear el desempeño e identificar al instante las áreas que requieren atención. Esto va más allá de los procesos manuales y proporciona información en tiempo real.
Fomentar una cultura de comunicación abierta.Anima a los miembros del equipo a identificar y comunicar proactivamente cualquier desviación o inquietud. Es vital fomentar una cultura sin culpas; concéntrate en aprender de los errores y mejorar los procesos. Convierte la lista de verificación en una herramienta para el crecimiento colectivo, no en una fuente de ansiedad.
7. Realizar un seguimiento de las tendencias y analizar datos: No te limites a marcar casillas; ¡analiza los datos! Identifica problemas recurrentes, realiza un seguimiento de las métricas de rendimiento y utiliza esta información para impulsar mejoras en los procesos y perfeccionar tu programa de BPL. Un documento estático se transforma en una herramienta dinámica para la mejora continua de la calidad.
Recursos y Enlaces
- U.S. Food and Drug Administration (FDA) : The FDA is the primary regulatory body overseeing GLP compliance in the US. Their website provides regulations, guidance documents, and information related to GLP.
- U.S. Environmental Protection Agency (EPA) : The EPA also regulates GLP, particularly related to environmental testing. Their site offers relevant guidance and resources.
- Organisation for Economic Co-operation and Development (OECD) : The OECD provides internationally harmonized GLP principles. This is a key resource for understanding the global perspective on GLP.
- United States Pharmacopeia (USP) : USP provides standards and resources related to quality assurance and control, which are highly relevant to GLP implementation. While not solely focused on GLP, their materials offer valuable insights.
- Pharmaceutical and Medical Devices Agency (PMDA) - Japan : Provides information and guidelines related to GLP as implemented in Japan. Offers a different regional perspective on GLP regulations.
- International Organization for Standardization (ISO) : ISO provides standards and guidelines applicable to quality management systems, many of which align with GLP principles. ISO 9001, in particular, is relevant.
- ASTM International : ASTM develops and publishes voluntary consensus standards used globally. While not exclusively GLP focused, their standards often cover aspects like equipment calibration and validation, which are crucial for GLP compliance.
- NiceQuest : Provides GLP training courses and resources. A commercial offering, but often provides a good overview of GLP principles and requirements.
- ComplianceBridge : Offers GLP consulting, training, and software solutions. Provides practical guidance and support for GLP implementation.
- Global GMP : A resource offering news, regulatory updates, and training related to GMP and GLP. Provides a broad perspective on compliance.
- QSA, Inc. : Provides GLP audits and consulting services. They offer valuable insights into common GLP deficiencies and best practices.
- EMC2 Group : Consulting firm specializing in regulatory compliance, including GLP. Offers training and auditing services.
- SPS Compliance : Provides GLP consulting, auditing, and training services. Focused on helping companies achieve and maintain GLP compliance.
Preguntas frecuentes
¿Qué significa GLP y por qué es importante?
GLP significa Buenas Prácticas de Laboratorio. Es un sistema de calidad diseñado para garantizar la fiabilidad y la integridad de los estudios de laboratorio no clínicos, especialmente aquellos que respaldan las presentaciones regulatorias (como las de fármacos o pesticidas). El cumplimiento de los principios de GLP asegura que los datos sean precisos, trazables y confiables.
¿Quién necesita usar una lista de verificación GLP?
Cualquier persona involucrada en la ejecución o gestión de estudios de laboratorio no clínicos que deban cumplir con las regulaciones de BPL. Esto incluye a los responsables de laboratorio, directores de estudio, personal de estudio, gestores de datos y personal de aseguramiento de la calidad.
¿Qué incluye la plantilla de su lista de verificación de GLP?
Nuestra plantilla abarca áreas clave del cumplimiento de las BPL, incluyendo el mantenimiento de instalaciones y equipos, los procedimientos operativos estándar (POE), la capacitación del personal, la gestión de datos, la ejecución de los estudios y las actividades de aseguramiento de la calidad. Está diseñada para ser adaptable a diferentes tipos de estudio y a las necesidades organizativas.
¿Es personalizable esta plantilla de lista de verificación?
¡Sí! La plantilla está diseñada para ser un punto de partida. Puede añadir, eliminar o modificar elementos fácilmente para adaptarla a sus protocolos de estudio, procedimientos operativos estándar (SOP) y requisitos reglamentarios específicos. Animamos a los usuarios a personalizarla para que se ajuste mejor a sus necesidades.
¿En qué formato de archivo está disponible la plantilla de la lista de verificación?
La plantilla de lista de verificación se proporciona en formato Microsoft Excel (.xlsx), lo que permite una edición, seguimiento y registro de datos sencillos.
¿Cómo puedo usar la plantilla de lista de verificación de manera efectiva?
1. Revise los elementos de la lista de verificación y comprenda los principios subyacentes de las BPL. 2. Adapte la lista de verificación para que refleje sus protocolos de estudio y procedimientos operativos estándar específicos. 3. Utilícela durante la planificación, ejecución y cierre del estudio. 4. Documente todas las acciones realizadas y cualquier desviación de la lista de verificación. 5. Revise y actualice periódicamente la lista de verificación para garantizar su eficacia continua.
¿Cuál es el papel del Director de Estudios en relación con la lista de verificación de BPL?
El Director del Estudio es, en última instancia, responsable de garantizar el cumplimiento de las BPL. Debe participar activamente en el proceso de la lista de verificación, revisar las listas de verificación completadas y abordar cualquier deficiencia identificada. La lista de verificación sirve como una herramienta valiosa para que el Director del Estudio monitoree el cumplimiento y mantenga la integridad de los datos.
¿Qué ocurre si encuentro una deficiencia utilizando la lista de verificación?
Cualquier deficiencia identificada debe ser documentada, investigada y corregida. Se debe desarrollar e implementar un plan de acciones correctivas para prevenir la recurrencia. La documentación de la lista de verificación debe describir claramente la deficiencia, las acciones correctivas adoptadas y la verificación de su eficacia.
¿Puede esta lista de verificación utilizarse para estudios no directamente relacionados con las presentaciones regulatorias?
Si bien está diseñado teniendo en cuenta el cumplimiento normativo, la lista de verificación puede adaptarse para su uso en cualquier estudio de laboratorio donde la calidad de los datos y la trazabilidad sean esenciales, incluso si no se presenta directamente a las autoridades reguladoras.
¿Te resultó útil este artículo?
Demostración de la solución de gestión de la fabricación
¡Deje de lidiar con papeleo y sistemas desconectados! Nuestra solución aporta claridad y control a su proceso de producción. Desde procedimientos operativos estándar (SOP) y mantenimiento de equipos hasta control de calidad y seguimiento de inventario, simplificamos cada paso.
Artículos relacionados
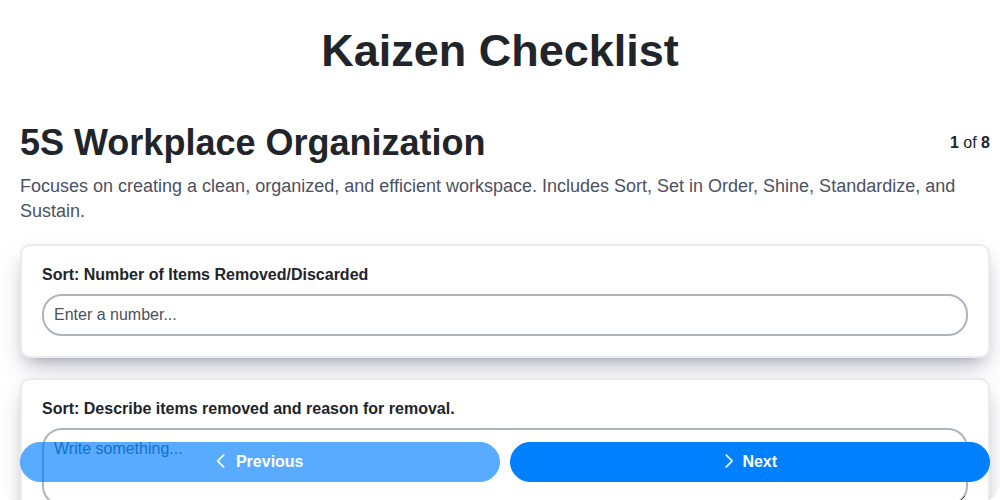
Plantilla de lista de verificación Kaizen: Su camino hacia la mejora continua

Machine Safety Audit Checklist: Your Guide to a Safer Manufacturing Workplace
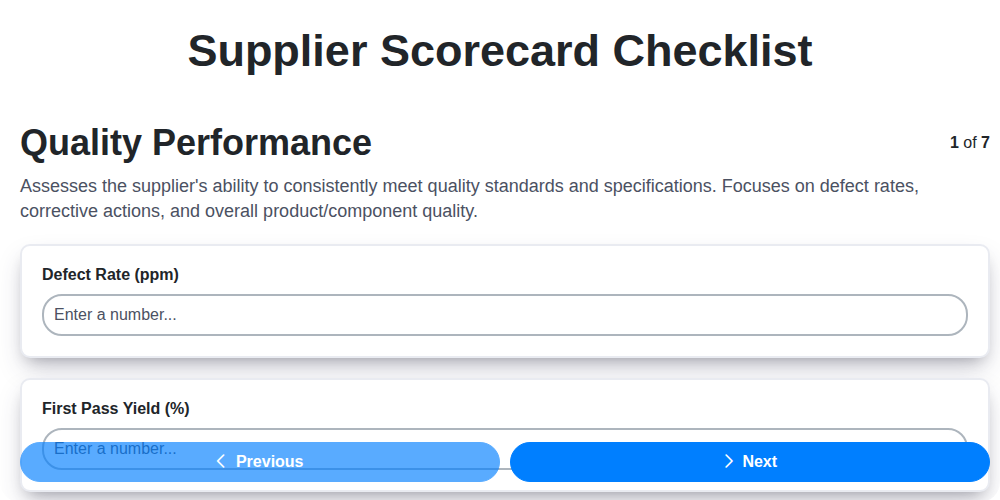
Mastering Supplier Performance: Your Free Supplier Scorecard Checklist Template
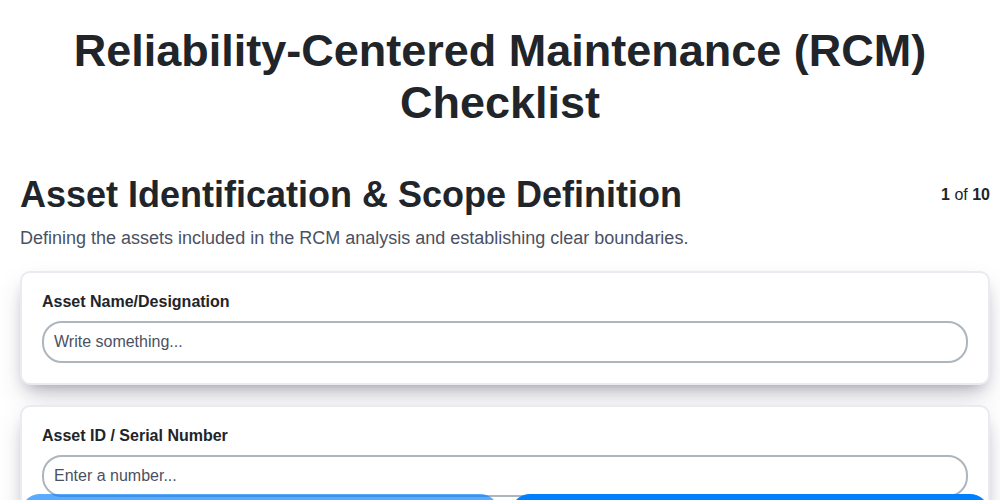
Tu plantilla definitiva de lista de verificación de RCM: Una guía paso a paso

Plantilla de verificación LPA: Su guía para auditorías de procesos por capas

Tu plantilla definitiva de control de aislamiento energético (LOTO)

Your Ultimate FSC 22000 Checklist Template
Plantilla de Lista de Verificación para Inspección de Control de Calidad: Prevenir Defectos y Mejorar los Procesos de Fabricación
Podemos hacerlo juntos
¿Necesita ayuda con las listas de verificación?
¿Tienes alguna pregunta? Estamos aquí para ayudarte. Envía tu consulta y te responderemos a la brevedad.