Twoja niezbędna lista kontrolna GMP: przewodnik krok po kroku
Opublikowano: 09/02/2025 Zaktualizowano: 04/10/2026
Spis treści
- Zrozumienie podstaw: Co to jest lista kontrolna GMP? (I dlaczego ona jest potrzebna)
- Określanie zakresu - dopasowanie listy kontrolnej do Państwa działalności
- Zasoby Ludzkie i Szkolenia - Budowanie Wykwalifikowanego Zespołu
- Utrzymanie Kontrolowanego Środowiska - Obiekty i Wyposażenie
- Dokumentacja i Archiwizacja - Zapewnienie Śledzenia
- Surowce i komponenty - jakość od początku.
- Kontrola Procesu Produkcyjnego - Zapewnienie Ciągłości Realizacji
- Zarządzanie odchyleniami i CAPA - wyciąganie wniosków z błędów
- Zarządzanie zmianą - efektywne zarządzanie modyfikacjami
- Wdrażanie i weryfikacja listy kontrolnej: działanie w praktyce.
- Zasoby i linki
TL;DR: Pobierz bezpłatny, konfigurowalny szablon listy kontrolnej GMP, aby upewnić się, że Twoje procesy produkcyjne spełniają standardy jakości. Ten przewodnik krok po kroku wyjaśnia zakres każdej sekcji - od szkolenia personelu po kontrolę zmian - dzięki czemu możesz łatwo dostosować go do swojej branży i zapewnić zgodność!
Zrozumienie podstaw: Co to jest lista kontrolna GMP? (I dlaczego ona jest potrzebna)
Lista kontrolna GMP to nie tylko dokument; to praktyczne odzwierciedlenie Państwa zaangażowania w jakość i zgodność z przepisami. Wyobraźcie sobie ją jako ustrukturyzowany, krok po kroku przewodnik, który zapewnia, że każdy kluczowy proces w Państwa procesie produkcyjnym jest konsekwentnie realizowany zgodnie z ustalonymi procedurami i wytycznymi regulacyjnymi.
W swojej istocie, lista kontrolna GMP szczegółowo opisuje konkretne działania, weryfikacje i dokumentację wymagane na każdym etapie procesu produkcyjnego - od przyjmowania surowców po dopuszczenie gotowych wyrobów. Te elementy nie są przypadkowe; są starannie wybrane, aby uwzględnić potencjalne ryzyko i zapewnić bezpieczeństwo, skuteczność i spójność produktu.
Dlaczego to jest tak ważne? Ponieważ przepisy GMP, choć wyczerpujące, mogą przytłaczać. Lista kontrolna przekształca te często skomplikowane wymagania w konkretne kroki, minimalizując ryzyko błędów ludzkich, promując identyfikowalność i dostarczając namacalnych dowodów zgodności z najlepszymi praktykami. To coś więcej niż tylko odhaczanie pól; to proaktywne działanie, które buduje kulturę jakości w całej organizacji.
Określanie zakresu - dopasowanie listy kontrolnej do Państwa działalności
Uniwersalna lista kontrolna GMP, choć stanowi dobry punkt wyjścia, rzadko jest wystarczająca sama w sobie. Prawdziwa siła tkwi w jej dostosowywaniu - precyzyjnym dopasowaniu do konkretnych operacji i wymogów regulacyjnych. Zanim zaczniesz oznaczać poszczególne punkty, przeprowadź dokładny spis swoich procesów.
Zacznij od zmapowania każdego etapu cyklu produkcyjnego - od przyjęcia surowców do wypuszczenia gotowego produktu. Zidentyfikuj kluczowe punkty kontroli (KPZ) na każdym etapie; są to punkty, w których odchylenia mogą znacząco wpłynąć na jakość i bezpieczeństwo produktu. Nie pomijaj pozornie drobnych procesów - nawet zadania administracyjne mogą być kluczowe.
Rozważ otoczenie regulacyjne. Które wytyczne GMP mają zastosowanie do Twojej branży i produkowanych przez Ciebie produktów? (np. 21 CFR Part 210 & 211 dla farmaceutyków w USA, wytyczne GMP UE, BRCGS dla przemysłu spożywczego). Te przepisy określają konkretne wymagania, które muszą zostać uwzględnione w Twojej liście kontrolnej.
Wreszcie, zastanów się nad unikalnymi cechami Twojej firmy - rodzajami używanego sprzętu, skalą działalności oraz specyficznymi zagrożeniami związanymi z procesami. Twoja lista kontrolna powinna odzwierciedlać te elementy, aby zapewnić naprawdę skuteczowy i odpowiedni przewodnik po zgodności z GMP. To wstępne określenie zakresu stworzy podstawę pod solidną i dopasowaną listę kontrolną GMP, która realnie zabezpieczy Twoją firmę i Twoich klientów.
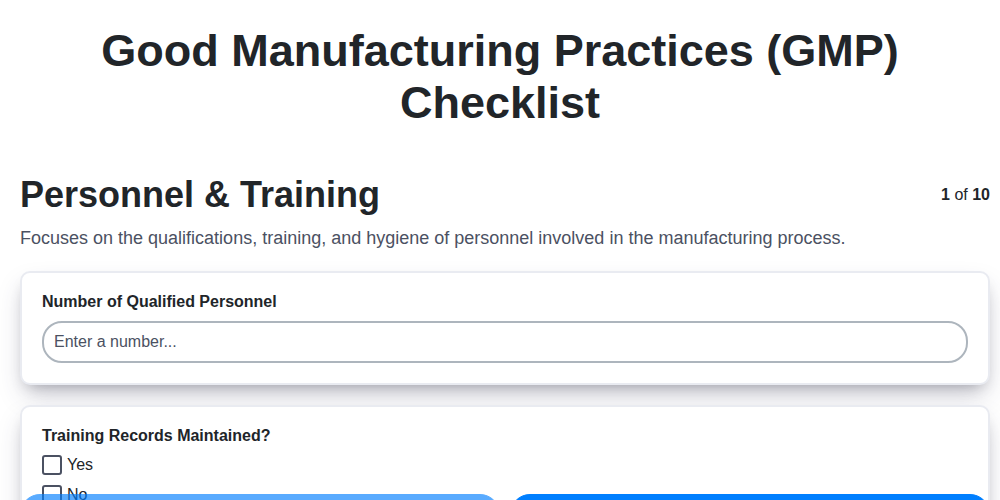
Zasoby Ludzkie i Szkolenia - Budowanie Wykwalifikowanego Zespołu
Solidny system GMP rozpoczyna się od dobrze przeszkolonego i kompetentnego zespołu pracowników. Personel stanowi podstawę każdej działalności produkcyjnej, a ich zrozumienie zasad GMP bezpośrednio wpływa na jakość produktu i bezpieczeństwo pacjentów/konsumentów. Samo zatrudnienie nie wystarczy; kluczowe jest ciągłe szkolenie i weryfikacja ich wiedzy.
Kluczowe punkty kontrolne i uwagi:
- Wstępne szkolenie: Wszyscy pracownicy zaangażowani w produkcję, przetwarzanie, pakowanie, etykietowanie i kontrolę jakości powinni przejść gruntowne wstępne szkolenie obejmujące podstawy GMP, obowiązujące procedury operacyjne (SOP) oraz zasady higieny. Powinno ono zawierać pokazy praktyczne i oceny.
- Szkolenia dostosowane do konkretnych ról.Oprócz ogólnej świadomości zasad GMP, szkolenia muszą być dostosowane do konkretnych stanowisk i obowiązków. Analityk kontroli jakości wymaga innych umiejętności i wiedzy niż pracownik produkcji.
- Dokumentacja jest najważniejsza.Należy prowadzić szczegółowe rejestry wszystkich szkoleń, zawierające daty, tematykę, wyniki ocen oraz podpisy osób uczestniczących. Te rejestry stanowią dowód zgodności z wymaganiami i mogą być kluczowe podczas audytów.
- Ocena kompetencji: Nie tylkodostarczyćszkoleniezweryfikować Zrozumienie. Wprowadź regularne oceny kompetencji (egzaminy pisemne, pokazy praktyczne, obserwacje), aby zapewnić, że personel efektywnie wykorzystuje swoją wiedzę.
- Szkolenie odświeżające: GMP stale się nieustannie rozwija, a procesy ulegają zmianom. Planowane szkolenia przypominające (lub odświeżające) utrzymują pracowników na bieżąco z nowymi przepisami, procedurami i najlepszymi praktykami. Częstotliwość zależy od stanowiska i zmieniających się wymagań.
- Higiena i praktyki dotyczące osobistej pielęgnacji: Wzmocnij znaczenie osobistej higieny i bezpiecznych praktyk pracy. Obejmuje to mycie rąk, prawidłowe stosowanie środków ochrony indywidualnej (ŚOI) oraz zgłaszanie wszelkich problemów zdrowotnych, które mogłyby wpłynąć na bezpieczeństwo produktu.
- Szkolenie podwykonawców: Nie zapominajmy o podwykonawcach ani o pracownikach tymczasowych! Muszą oni otrzymać odpowiednie szkolenie GMP, dostosowane do powierzonych im zadań, często odpowiadające szkoleniu przeznaczonemu dla pracowników stałych.
- Zasady przechowywania dokumentów: Ustanów wyraźne procedury dotyczące przechowywania dokumentacji szkoleniowej przez wymagany okres, zgodnie z wytycznymi regulacyjnymi.
Dobrze wyszkolony zespół to pierwsza linia obrony przed problemami z jakością - inwestuj w ich rozwój i zapewnij im wiedzę i umiejętności, które pozwolą na konsekwentne wytwarzanie bezpiecznych i skutecznych produktów.
Utrzymanie Kontrolowanego Środowiska - Obiekty i Wyposażenie
Skuteczny system GMP zależy od integralności zakładu i niezawodności urządzeń. Obejmuje to znacznie więcej niż tylko czysta przestrzeń; chodzi o tworzenie i utrzymywanie kontrolowanego środowiska, które minimalizuje ryzyko zanieczyszczeń, krzyżowych zanieczyszczeń i błędów.
Rozważania dotyczące obiektów/infrastruktury.
Projekt i układ Twojego obiektu odgrywają kluczową rolę. Należy wziąć pod uwagę następujące istotne kwestie:
- Kontrolowany dostęp: Ogranicz dostęp do obszarów produkcyjnych wyłącznie do upoważnionego personelu. Wprowadź solidne środki bezpieczeństwa i procedury dotyczące odwiedzających.
- Odpowiednia wentylacja i wentylacja powietrza.Zapewnij odpowiednią wentylację i systemy filtracji powietrza w celu zminimalizowania zanieczyszczeń przenoszonych drogą powietrzną. Regularnie monitoruj i konserwuj te systemy, w tym filtry HEPA, jeśli dotyczy.
- Wyodrębnienie działań: Wyraźnie zdefiniuj i wydziel strefy w oparciu o ryzyko, takie jak magazynowanie surowców, przetwarzanie, pakowanie i kwarantanna. Zapobiegaj krzyżowym zakażeniom między tymi strefami.
- Zwalczanie szkodników: Wprowadź kompleksowy program zwalczania szkodników w celu zapobiegania infestacjom. Obejmuje to rutynowe przeglądy, pułapki oraz działania zapobiegawcze. Dokumentuj wszystkie czynności skrupulatnie.
- Materiały wykończeniowe: Wykorzystuj materiały trwałe, nie pylące, łatwe do czyszczenia i odporne na chemikalia stosowane w Twoich procesach. Unikaj materiałów porowatych, jeśli to możliwe.
- Oświetlenie: Odpowiednie i właściwe oświetlenie jest niezbędne dla widoczności i bezpieczeństwa operatora.
Niezawodność sprzętu:
Jakość Twojego sprzętu jest równie dobra, co jego utrzymanie. Kluczowe znaczenie ma proaktywne podejście do zarządzania sprzętem.
- Harmonogramy Przeglądów Zapobiegawczych: Ustanów i rygorystycznie przestrzegaj harmonogramów konserwacji zapobiegawczej dla wszystkich kluczowych urządzeń. Udokumentuj wszystkie czynności konserwacyjne.
- Kalibracja i walidacja: Regularnie kalibruj i weryfikuj urządzenia, aby zapewnić dokładność i niezawodność. Prowadź szczegółowe rejestry tych czynności.
- Projektowanie sprzętu i materiały: Wybierz sprzęt wykonany z materiałów kompatybilnych z produktami i środkami czyszczenia, które są używane.
- Czyszczenie i dezynfekcja: Opracuj i zweryfikuj solidne procedury czyszczenia i dezynfekcji dla wszystkich urządzeń. Udokumentuj te procedury i potwierdź ich skuteczność.
- Kwalifikacja sprzętu: Należy upewnić się, że wszystkie nowe urządzenia są odpowiednio zweryfikowane przed użyciem, potwierdzając ich prawidłowe działanie i spełnianie wszystkich wymagań. Obejmuje to kwalifikację instalacyjną (IQ), kwalifikację operacyjną (OQ) oraz kwalifikację wydajnościową (PQ).
- Zarządzanie zmianą dla urządzeń: Wszelkie modyfikacje lub naprawy urządzeń powinny być starannie zarządzane za pomocą systemu kontroli zmian, aby zapewnić, że nie wpłyną one na jakość produktu ani walidację procesu.
Dokumentacja i Archiwizacja - Zapewnienie Śledzenia
Solidna dokumentacja to nie tylko wypełnianie formalności; to kręgosłup zgodnego z przepisami i efektywnego systemu GMP. Każdy etap, od przyjęcia surowców po zwolnienie gotowego produktu, powinien być skrupulatnie udokumentowany i łatwo dostępny. Wyobraźcie sobie waszą dokumentację jako szczegółową historię podróży waszego produktu - historię, którą każdy, w tym audytorzy, musi być w stanie zrozumieć.
Dlaczego to jest tak ważne?Śledzenie pochodzenia. W przypadku odwołania, dochodzenia lub problemu z jakością, kompletne i dokładne dokumenty pozwalają szybko zidentyfikować przyczynę problemu, ocenić jego wpływ i wdrożyć działania naprawcze. Bez tego działasz na oślep.
Co wymaga udokumentowania? Lista jest obszerna, ale kluczowe obszary obejmują:
- Procedury Operacyjne (PO) Szczegółowe instrukcje dla wszystkich procesów, regularnie weryfikowane i zatwierdzane.
- Karty seriiKompletne dokumenty każdej partii produkcyjnej, zawierające informacje o użytych surowcach, ustawieniach urządzeń, czynnościach operatora oraz wynikach testów.
- Dokumentacja kalibracji i konserwacji sprzętu: Dowód prawidłowego działania sprzętu i zgodności z wymaganiami.
- Ewidencja Szkoleń: Dokumentacja szkoleń pracowników, potwierdzająca ich kompetencje w wykonywanych rolach.
- Raporty odchyleń: Zapisy wszelkich odchyleń od ustalonych procedur, w tym wyniki dochodzeń i podjęte działania naprawcze.
- Karty zmian.Dokumentacja wszelkich zmian w procesach, urządzeniach lub materiałach, wraz z oceną wpływu i zatwierdzeniami.
Kluczowe zasady skutecznego prowadzenia dokumentacji:
- Dokładność: Zapewnij, aby dane były dokładne, kompletne i czytelne.
- Kolejność chronologicznaNależy prowadzić dokumentację w porządku chronologicznym.
- Oryginalne zapisy: Należy przechowywać oryginalne dokumenty (lub ich urzędowo potwierdzone kopie).
- Ograniczony dostęp: Ogranicz dostęp do dokumentów do upoważnionego personelu.
- Bezpieczne przechowywanie: Przechowuj dokumenty w bezpiecznym i kontrolowanym klimatycznie środowisku.
- Regularne przeglądy: Regularnie sprawdzaj dokumenty pod kątem dokładności i kompletności.
- Dokumenty Elektroniczne: Korzystając z dokumentacji elektronicznej, należy zapewnić, aby systemy były zweryfikowane i zgodne z obowiązującymi przepisami (np. część 21 CFR 11 dla produktów farmaceutycznych w USA).
Surowce i komponenty - jakość od początku.
Przysłowie mówiące, że z wieprzowego ucha nie uszyjesz jedwabnej torebki, znajduje odzwierciedlenie w produkcji. Jakość gotowego produktu jest nierozerwalnie związana z jakością surowców i elementów użytych do jego wytworzenia. Solidny program zarządzania surowcami to nie tylko wymóg regulacyjny, ale fundament skutecznego systemu jakości.
W tej sekcji skupiono się na wprowadzeniu kontroli, które zapewnią, że do procesu produkcyjnego trafią tylko odpowiednie materiały. Chodzi nie tylko o składanie zamówień u dostawcy; obejmuje to cały cykl życia komponentu, od wstępnego pozyskania do zużycia.
Kluczowe elementy programu kontroli surowców i komponentów:
- Kwalifikacja Dostawców: Nie wybieraj dostawcy wyłącznie ze względu na cenę. Wprowadź rygorystyczny proces kwalifikacji, obejmujący audyty (zarówno zapowiedziane, jak i nieplanowane), weryfikację systemów jakości oraz sprawdzenie zgodności z obowiązującymi przepisami. To buduje zaufanie i odpowiedzialność.
- Wchodzące Kontrole i Testy: Każda partia dostarczanych materiałów powinna zostać poddana kontroli i badaniom, zgodnie z ustalonymi specyfikacjami. Obejmuje to inspekcje wzrokowe, badania analityczne (np. czystość, tożsamość, moc) oraz, w zależności od materiału, potencjalnie nawet ocenę sensoryczną. Niezbędne są jasno określone plany pobierania próbek.
- Identyfikacja materiałów i identyfikowalność.Wprowadź system umożliwiający jasną identyfikację i śledzenie każdej partii materiałowej do dostawcy oraz powiązanej dokumentacji. Unikalne numery partii, skanowanie kodów kreskowych oraz elektroniczne systemy śledzenia to cenne narzędzia.
- Kwarantanna i UwolnienieWchodzące materiały powinny być poddawane kwarantannie do czasu ich przeglądu, testowania i dopuszczenia do użytku. Jasna procedura dopuszczania, udokumentowana przez upoważnione osoby, zapobiega przypadkowemu wykorzystaniu materiałów niezgodnych ze specyfikacją.
- Warunki przechowywania: Odpowiednie warunki przechowywania są kluczowe dla zachowania integralności materiału. Należy kontrolować temperaturę, wilgotność, działanie światła oraz inne czynniki środowiskowe, zgodnie z zaleceniami podanymi w karcie danych materiału.
- Status materiału i okres przydatności. Monitoruj status materiałów (np. kwarantanna, zatwierdzone, przeterminowane) i rzetelnie zarządzaj datą ważności. Należy ściśle przestrzegać zasady pierwsze weszło, pierwsze wyszło (FIFO).
- Zarządzanie niezgodnościamiNależy ustalić jasną procedurę postępowania z materiałami niezgodnymi, obejmującą dokumentację, badanie przyczyn i wyodrębnienie. Odrzucone materiały powinny zostać zwrócone dostawcy lub zutylizowane w odpowiedni sposób.
Wdrażając te środki kontroli, tworzysz solidne podstawy dla jakości i minimalizujesz ryzyko wad produktu wynikających z materiałów surowych niskiej jakości.
Kontrola Procesu Produkcyjnego - Zapewnienie Ciągłości Realizacji
Kontrola procesu produkcyjnego jest podstawą wysokiej jakości produkcji. Samo to nie wystarczy, by...miećZweryfikowane procesy wymagają konsekwentnego wdrażania. Oznacza to zapewnienie, że każda partia, każdy etap, jest realizowany zgodnie z ustalonymi procedurami, a wszelkie odchylenia są niezwłocznie wykrywane i rozwiązywane.
Wyobraź sobie to jak przepis - nawet najlepszy przepis jest bezużyteczny, jeśli składniki są odmierzone nieprawidłowo lub czas gotowania jest błędny. Podobnie, solidne Procedury Operacyjne (SOP) są skuteczne tylko wtedy, gdy są przestrzegane skrupulatnie.
Kluczowe elementy zapewniające spójne realizowanie zadań:
- Testowanie w trakcie realizacji: Regularnie monitoruj krytyczne parametry (temperatura, pH, lepkość, itd.) na każdym etapie procesu produkcyjnego. Wprowadź jasny harmonogram testów i zapewnij, aby wyniki były dokładnie rejestrowane i oceniane.
- Dokumentacja serii produkcji. Poniżej znajdują się szczegółowe kroniki procesu produkcyjnego. Powinny one dokumentowaćwszystko- od numerów partii surowców po ustawienia urządzeń i inicjały operatora. Dokładne i kompletne dokumentacje serii są niezbędne dla identyfikowalności i dochodzeń.
- Szkolenie i kompetencje operatorów. Osoby wykonujące czynności produkcyjne muszą być odpowiednio przeszkolone i wykazać kompetencje w ich realizacji. Nie jest to jednorazowe zdarzenie; ciągłe szkolenia i powtórki są niezbędne.
- Kalibracja i konserwacja sprzętu: Regularnie skalibrowane i konserwowane urządzenia zapewniają niezawodne i powtarzalne działanie, minimalizując zmienność w Twoim procesie.
- Zarządzanie odchyleniamiKażde odstępstwo od ustalonych procedur musi być udokumentowane, zbadane i rozwiązane niezwłocznie. Pomaga to zidentyfikować potencjalne problemy i zapobiec ich powtórzeniu.
- Monitorowanie w czasie rzeczywistym (jeśli dotyczy): Wdrożenie systemów monitoringu w czasie rzeczywistym może zapewnić natychmiastowe powiadomienia o odchyleniach i umożliwić podejmowanie proaktywnych działań korygujących. Jest to szczególnie cenne w przypadku procesów o wysokiej wrażliwości.
Spójność to nie tylko przestrzeganie zasad; to wdrożenie jakości w każdy aspekt procesu produkcyjnego.
Zarządzanie odchyleniami i CAPA - wyciąganie wniosków z błędów
Odchylenia - te nieplanowane odstępstwa od ustalonych procedur - są nieuniknione w każdym procesie produkcyjnym. Kluczem nie jest ich całkowite wyeliminowanie (nerealny cel!), lecz stworzenie solidnego systemu identyfikacji, analizy i rozwiązywania tych odchyleń. Właśnie tutaj do gry wchodzą Zarządzanie Odchyleniami oraz Działania Korekcyjne i Zapobiegawcze (CAPA). Wyobraźcie to sobie jako pętlę uczenia się: zdarza się błąd, rozumiecie, dlaczego do niego doszło, go naprawiacie i zapobiegacie jego powtórzeniu.
Dobrze skonstruowany system zarządzania odchyleniami obejmuje jasne procedury raportowania, zapewniające, że każda odchyła - niezależnie od tego, jak wydaje się ona drobna - jest dokumentowana natychmiast. Ten zapis powinien zawierać szczegóły takie jak data, godzina, opis odchylenia, osoby zaangażowane oraz podjęte natychmiastowe działanie korygujące. Nie lekceważ drobnych odchyleń; mogą one być wczesnymi sygnałami ostrzegającymi o poważniejszych problemach systemowych.
Faza śledztwa jest kluczowa. Wymaga ona dokładnej analizy przyczyn źródłowych, aby ustalićdlaczegoWystąpiło odchylenie. Samo leczenie objawu to za mało; trzeba zrozumieć przyczynę leżącą u jego podłoża. Czy to problem z wyszkoleniem, uszkodzone urządzenie, luka w procedurze, czy coś zupełnie innego? Wykorzystanie narzędzi, takich jak technika 5 Dlaczego, może być bardzo pomocne w dogłębnej analizie.
Gdy już zostanie zidentyfikowana przyczyna źródłowa, działanie korygujące ma na celu rozwiązanie konkretnego problemu. Działania zapobiegawcze, z drugiej strony, to proaktywne kroki podejmowane w celu uniknięcia podobnych odchyleń w przyszłości. Oba rodzaje działań muszą być wyraźnie udokumentowane, wdrożone i monitorowane.
Kluczowe jest zweryfikowanie skuteczności działań korygujących i zapobiegawczych. Czy działania rzeczywiście rozwiązały problem i zapobiegły jego powtórzeniu? Regularny przegląd danych dotyczących odchyleń oraz skuteczności działań korygujących i zapobiegawczych jest niezbędny dla ciągłego doskonalenia systemu jakości. Solidny system działań korygujących i zapobiegawczych przekształca odchylenia z potencjalnych przeszkód w cenne możliwości nauki i rozwoju.
Zarządzanie zmianą - efektywne zarządzanie modyfikacjami
Zmiany są nieuniknione w każdym środowisku produkcyjnym. Niezależnie od tego, czy to drobna zmiana w procesie, modernizacja sprzętu czy modyfikacja surowców, zmiany mogą wpływać na jakość i bezpieczeństwo produktu. Właśnie dlatego solidny system kontroli zmian staje się absolutnie niezbędny. Chodzi nie tylko o wprowadzanie zmian, ale o ich zarządzanie.skutecznieaby zminimalizować ryzyko i utrzymać zgodność.
Dobrze zdefiniowany proces zarządzania zmianą zapewnia, że każda proponowana modyfikacja przechodzi dokładną ocenę przed wdrożeniem. Ocena ta powinna uwzględniać potencjalny wpływ na jakość produktu, walidację procesu, kwalifikację wyposażenia i dokumentację. Jest to wieloaspektowe podejście, angażujące wkład z różnych działów - produkcji, zapewnienia jakości, działu technicznego i potencjalnie innych - w celu uzyskania kompleksowego obrazu zmiany.
Kluczowe elementy skutecznego systemu kontroli zmian obejmują:
- Inicjacja wniosku o zmianę: Formalny system zgłaszania proponowanych zmian, wyraźnie określający uzasadnienie, zakres i oczekiwany wpływ.
- Ocena wpływuSzczegółowa analiza wpływu tej zmiany na różne aspekty procesu produkcyjnego, w tym na jakość, bezpieczeństwo i zgodność z przepisami.
- Ocena ryzyka: Identyfikacja i ocena potencjalnych ryzyk związanych z wprowadzaną zmianą oraz opracowanie strategii ich łagodzenia.
- Przepływ zatwierdzania. Udokumentowany proces przeglądania i zatwierdzania zmian, obejmujący wyznaczone osoby posiadające uprawnienia i wiedzę specjalistyczną do podejmowania świadomych decyzji.
- Wdrożenie i Walidacja: Staranne wdrożenie zmiany, po którym następuje walidacja lub ponowna walidacja, aby zapewnić, że nie wpłynie ona negatywnie na jakość produktu.
- Dokumentacja i prowadzenie dokumentacji.Dokumentacja procesu zarządzania zmianą, obejmująca początkowe zgłoszenie, ocenę wpływu, analizę ryzyka, dokumentację zatwierdzeń oraz wyniki walidacji.
Brak wdrożenia solidnego systemu kontroli zmian może prowadzić do kosztownych błędów, wycofania produktów ze sprzedaży, kontroli regulacyjnych i uszczerbku na reputacji Twojej firmy. To proaktywna inwestycja w utrzymanie integralności procesów produkcyjnych oraz w wykazanie zaangażowania w jakość i zgodność z przepisami.
Wdrażanie i weryfikacja listy kontrolnej: działanie w praktyce.
Tworzenie listy kontrolnej GMP to dopiero połowa sukcesu. Prawdziwa wartość tkwi w konsekwentnymużywająci zapewnić jego skuteczność. Oto jak skutecznie zintegrować listę kontrolną z codziennymi operacjami i utrzymać jej zgodność z ewoluującymi wymaganiami.
Przydzielanie odpowiedzialności i szkolenia. Nie pozwól, aby Twoja lista kontrolna stała się zakurzonego rodzaju dokumentu. Przypisuj jasną odpowiedzialność za każdy punkt listy kontrolnej. Osoby lub zespoły powinny ponosić odpowiedzialność za przeprowadzanie kontroli, dokumentowanie wyników i zgłaszanie wszelkich problemów. Kluczowe jest zapewnienie kompleksowych szkoleń na temat prawidłowego wykonywania każdego punktu listy kontrolnej oraz zrozumienia leżących u jej podstaw zasad GMP. Niezbędne są regularne szkolenia odświeżające.
Zintegruj z przepływem pracy: Lista kontrolna nie powinna stanowić dodatkowego obciążenia. Zintegruj ją płynnie z istniejącymi procesami roboczymi. Może to obejmować włączenie pozycji z listy kontrolnej do standardowych procedur operacyjnych (SOP), wykorzystanie aplikacji do list kontrolnych lub powiązanie jej z dokumentacją serii. Zastanów się, jak zminimalizować zakłócenia, jednocześnie maksymalizując skuteczność.
3. Przyjmuj rozwiązania cyfrowe: Choć listy kontrolne w wersji papierowej mają swoje miejsce, rozwiązania cyfrowe oferują znaczące korzyści. Mogą automatyzować zbieranie danych, ułatwiać raportowanie w czasie rzeczywistym, poprawiać dokładność danych i upraszczać ścieżki audytowe. Zapoznaj się z opcjami takimi jak listy kontrolne oparte na tabletach, platformy w chmurze i systemy elektronicznej dokumentacji.
Regularny przegląd i audyt: Twoja lista kontrolna GMP nie jest dokumentem statycznym. Planuj regularne przeglądy - przynajmniej raz w roku, a idealnie częściej - aby zapewnić jej stałą aktualność. Przeprowadzaj wewnętrzne audyty w celu weryfikacji przestrzegania listy kontrolnej i identyfikacji obszarów wymagających poprawy. Porównuj wyniki z poprzednich okresów, aby monitorować wyniki i wykrywać trendy.
5. Przegląd zarządzania i ciągłe doskonalenie: Analiza wyników działania listy kontrolnej przez kierownictwo jest niezbędna. Zapewnia to platformę do omówienia ustaleń, ustalenia priorytetów działań naprawczych i aktualizacji listy kontrolnej w oparciu o wyciągnięte wnioski. Stwórz kulturę ciągłego doskonalenia, w której opinie z wszystkich szczebli organizacji są mile widziane i uwzględniane. Pamiętaj, że GMP to podróż, a nie cel.
Zasoby i linki
- FDA Biopharmaceutical CGMP Q&A : Official FDA guidance documents and frequently asked questions related to current Good Manufacturing Practices (cGMP) for biopharmaceutical products. A crucial resource for understanding regulatory expectations.
- ISO 211 - Pharmaceutical GxP Auditing : Provides a framework for auditing pharmaceutical quality systems and is frequently referenced when discussing GMP. Useful for understanding auditing standards.
- United States Pharmacopeia (USP) : Provides standards for pharmaceutical ingredients, excipients, and dosage forms. Relevant for ensuring quality and consistency in raw materials and finished products.
- American Society for Quality (ASQ) : A professional organization dedicated to quality. Provides resources, training, and publications related to quality management, including GMP principles.
- Pharmaceutical Online : Industry news, articles, and resources covering pharmaceutical manufacturing, quality, and regulatory compliance. Provides insights into current trends and best practices.
- GMP Compliance : Provides news, resources, and training focused specifically on GMP compliance. Offers practical advice and regulatory updates.
- ComplianceWorld : Offers a range of compliance resources, including articles, webinars, and training materials covering GMP and other regulated industries. Useful for keeping up with regulatory changes.
- EMC2 : Specializes in regulatory compliance software and services, including solutions for managing GMP documentation and training. Useful for understanding technology-driven solutions.
- MasterControl : Offers quality management system (QMS) software that often incorporates GMP compliance features. Provides insights into digital implementation of GMP processes.
- NSF International : Provides certification and testing services related to food, water, and pharmaceutical products. Relevant for ensuring compliance with specific standards and quality requirements.
- Centers for Disease Control and Prevention (CDC) : While broader, the CDC website can provide valuable information on contamination control, hygiene, and sanitation - critical aspects of maintaining a controlled facility environment.
Najczęściej zadawane pytania
Co oznacza skrót GMP i dlaczego jest ważny?
GMP to skrót od Dobrych Praktyk Produkcyjnych. Jest to system zapewniający, że produkty są konsekwentnie wytwarzane i kontrolowane zgodnie z normami jakości. Jest on niezbędny w branżach takich jak farmaceutyka, przemysł spożywczy i kosmetyczny, aby chronić bezpieczeństwo konsumentów i skuteczność produktów.
Kto powinien używać listy kontrolnej GMP?
Każda firma zajmująca się produkcją wyrobów podlegających regulacjom organu zarządzającego (np. FDA w USA) powinna korzystać z listy kontrolnej GMP. Dotyczy to producentów, dostawców i dystrybutorów.
Jakie rodzaje produktów zazwyczaj podlegają przepisom GMP?
Przepisy GMP często obejmują produkty farmaceutyczne, biologiczne produkty lecznicze, wyroby medyczne, produkty spożywcze, suplementy diety, kosmetyki oraz substancje czynne (API).
Co zawiera typowy szablon listy kontrolnej GMP?
Kompleksowa lista kontrolna GMP zazwyczaj obejmuje sekcje dotyczące szkolenia personelu, walidacji sprzętu, utrzymania budynków, kontroli dokumentacji, kontroli jakości, postępowania z surowcami oraz zarządzania odchyleniami.
Czy mogę zmodyfikować szablon listy kontrolnej GMP podany w artykule?
Tak, szablon został zaprojektowany do personalizacji. Należy go dostosować do specyficznych procesów, produktów i wymogów regulacyjnych. Regularnie przeglądaj i aktualizuj listę kontrolną, aby uwzględnić wszelkie zmiany.
Jaka jest różnica między listą kontrolną GMP a standardową procedurą operacyjną (SOP)?
Lista kontrolna GMP to dokument służący do weryfikacji przestrzegania standardowych procedur operacyjnych (SOP). SOP-y natomiast szczegółowo opisują, *jak* należy wykonać konkretne zadanie. Lista kontrolna potwierdza zgodność z SOP.
Jak często należy przeglądać i aktualizować listę kontrolną GMP?
Listy kontrolne GMP należy przeglądać i aktualizować co najmniej raz w roku lub częściej, jeśli występują istotne zmiany w procesach, przepisach lub wynikach audytów.
Co się dzieje, gdy audyt GMP wykaże niezgodności?
Niezgodności mogą skutkować pismami pouczeniowymi, wycofaniem produktów z rynku, zatrzymaniem importu, a nawet postępowaniem prawnym. Kluczowe jest szybkie reagowanie na uwagi poprzez podjęcie działań naprawczych i zapobiegawczych (CAPA).
Gdzie mogę znaleźć więcej informacji na temat przepisów GMP?
Szczegółowe informacje na temat przepisów GMP można znaleźć na stronach internetowych organów regulacyjnych, takich jak FDA (USA), EMA (Europa) oraz innych, specyficznych dla Państwa regionu i branży.
Jak mogę sprawdzić, czy moja lista kontrolna GMP jest naprawdę skuteczna?
Regularnie wykorzystuje się efektywną listę kontrolną, która jest aktualizowana na podstawie wyników audytów i zmian w procesach, oraz wykazuje stałe przestrzeganie wymagań GMP. Okresowe wewnętrzne audyty mogą pomóc w ocenie jej skuteczności.
Czy ten artykuł był pomocny?
Demo rozwiązania do zarządzania produkcją
Przestań tracić czas na papierkowanie i zmagania z niepowiązanymi systemami! Nasze rozwiązanie zapewnia jasność i kontrolę nad procesem produkcyjnym. Od standardowych procedur operacyjnych (SOP) i konserwacji sprzętu, po kontrolę jakości i śledzenie zapasów, upraszczamy każdy etap.
Powiązane artykuły
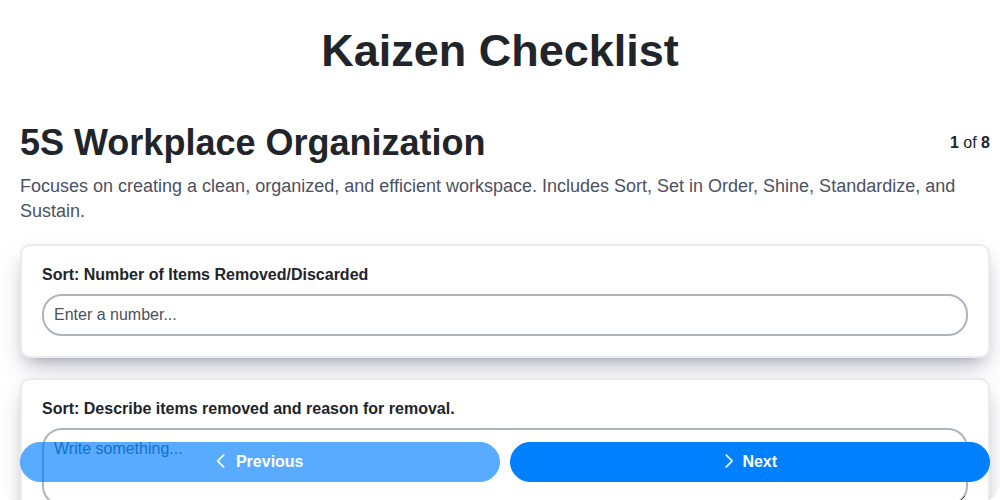
Szablon listy kontrolnej Kaizen: Twoja droga do ciągłego doskonalenia

Machine Safety Audit Checklist: Your Guide to a Safer Manufacturing Workplace
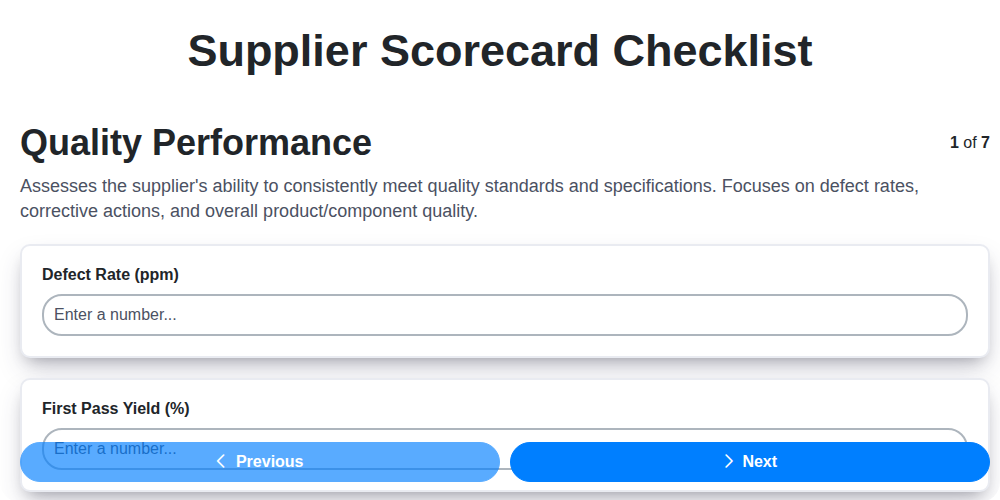
Mastering Supplier Performance: Your Free Supplier Scorecard Checklist Template
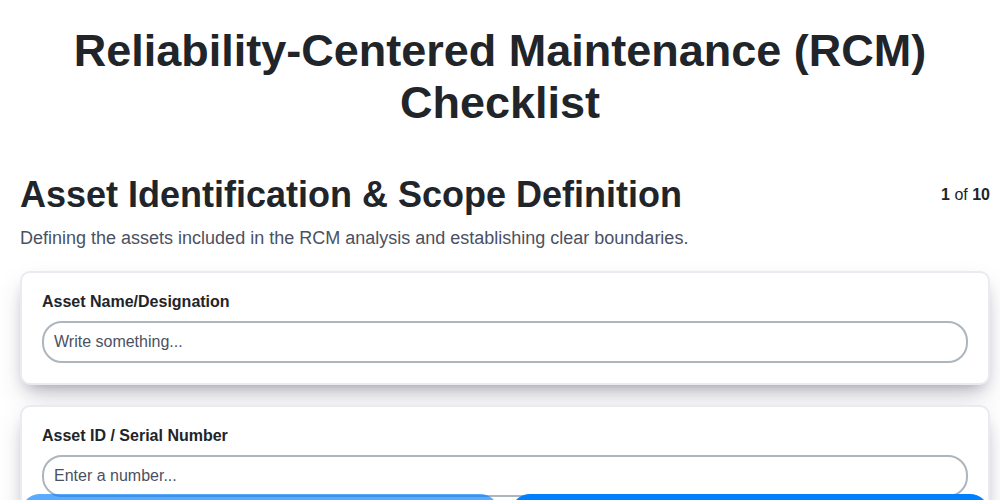
Twój ostateczny szablon listy kontrolnej RCM: Poradnik krok po kroku

Szablon listy kontrolnej LPA: Twój przewodnik po audytach procesów warstwowych

Twój kompleksowy szablon listy kontrolnej blokad i oznaczeń (LOTO).

Your Ultimate FSC 22000 Checklist Template
Szablon listy kontrolnej kontroli jakości: zapobiegaj wadom i ulepsz procesy produkcyjne.
Możemy to zrobić razem
Potrzebujesz pomocy z listami kontrolnymi?
Masz pytanie? Jesteśmy tu, aby pomóc. Prześlij zapytanie, a my szybko na nie odpowiemy.