Votre modèle de liste de contrôle GMP essentiel : un guide étape par étape
Publié: 09/02/2025 Mis à jour: 04/10/2026
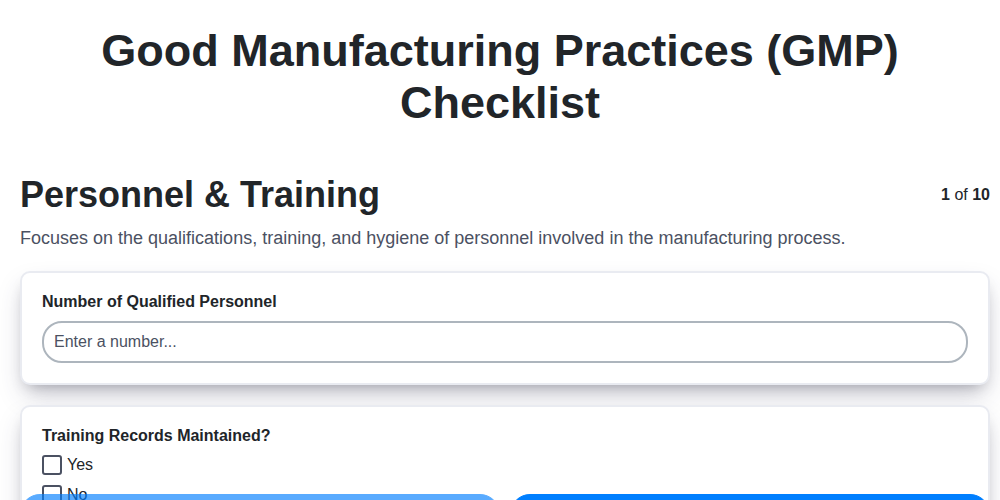
Table des matières
- Comprendre les bases : Qu'est-ce qu'une liste de contrôle BPF ? (Et pourquoi en avez-vous besoin)
- Définir votre périmètre - Adapter la liste de contrôle à vos opérations
- Personnel et Formation - Construire une Équipe Qualifiée
- Installations et équipements - Maintenir un environnement contrôlé
- Documentation et archivage - Garantir la traçabilité
- Matières premières et composants - Qualité dès le départ
- Contrôles des processus de fabrication - Exécution cohérente
- Gestion des écarts et CAPA - Tirer les leçons des erreurs
- Gestion des modifications - Piloter efficacement les changements
- Mise en œuvre et révision : passer à l'action avec votre liste de contrôle
- Ressources et liens
TL;DR : Obtenez un modèle de liste de contrôle GMP gratuit et personnalisable pour vous assurer que vos processus de fabrication respectent les normes de qualité. Ce guide vous explique le contenu de chaque section - de la formation du personnel au contrôle des modifications - afin que vous puissiez facilement l'adapter à votre secteur d'activité et rester conforme !
Comprendre les bases : Qu'est-ce qu'une liste de contrôle BPF ? (Et pourquoi en avez-vous besoin)
Une liste de contrôle GMP n'est pas qu'un document ; c'est la concrétisation pratique de votre engagement envers la qualité et la conformité réglementaire. Considérez-la comme un guide structuré, étape par étape, qui garantit que chaque processus critique au sein de votre opération de fabrication est exécuté de manière constante, conformément aux procédures établies et aux directives réglementaires.
Au fond, une liste de contrôle GMP détaille les actions, vérifications et enregistrements spécifiques requis à chaque étape de votre processus de fabrication, de la réception des matières premières à la mise en vente des produits finis. Ces éléments ne sont pas arbitraires ; ils sont soigneusement sélectionnés pour répondre aux risques potentiels et garantir la sécurité, l'efficacité et la constance des produits.
Pourquoi cela est-il si crucial ? Parce que les réglementations GMP, bien que complètes, peuvent être accablantes. Une liste de contrôle transforme ces exigences souvent complexes en étapes concrètes, réduisant ainsi le risque d'erreurs humaines, favorisant la traçabilité et fournissant une preuve tangible de votre conformité aux meilleures pratiques. Il ne s'agit pas simplement de cocher des cases ; c'est une mesure proactive qui instaure une culture de la qualité dans toute votre organisation.
Définir votre périmètre - Adapter la liste de contrôle à vos opérations
Une liste de contrôle GMP générique, bien qu'elle constitue un bon point de départ, est rarement suffisante en elle-même. La véritable force réside dans sa personnalisation : l'adapter précisément à vos opérations spécifiques et à vos obligations réglementaires. Avant de commencer à cocher les cases, faites d'abord l'inventaire complet de vos processus.
Commencez par cartographier chaque étape de votre cycle de fabrication, de la réception des matières premières à la mise en vente du produit fini. Identifiez les points critiques de contrôle (PCC) à chaque étape ; ce sont des points où des écarts pourraient avoir un impact significatif sur la qualité et la sécurité du produit. Ne négligez pas les processus qui peuvent paraître mineurs, même les tâches administratives peuvent être cruciales.
Tenez compte du contexte réglementaire. Quelles directives GMP sont applicables à votre secteur d'activité et aux produits que vous fabriquez ? (par exemple, 21 CFR Part 210 & 211 pour les produits pharmaceutiques américains, les directives GMP européennes, BRCGS pour l'alimentation). Ces réglementations définissent des exigences spécifiques qui doivent être prises en compte dans votre liste de contrôle.
Enfin, réfléchissez aux caractéristiques propres à votre entreprise : les types d'équipements utilisés, l'ampleur de vos opérations et les risques spécifiques liés à vos processus. Votre liste de contrôle devra refléter ces éléments afin de fournir un guide véritablement efficace et pertinent pour la conformité aux BPF. Cet exercice initial de définition du périmètre posera les bases d'une liste de contrôle BPF robuste et personnalisée, qui protégera véritablement votre entreprise et vos clients.
Personnel et Formation - Construire une Équipe Qualifiée
Un système GMP robuste commence par une main-d'œuvre bien formée et compétente. Le personnel est le pilier de toute opération de fabrication, et sa compréhension des principes GMP a un impact direct sur la qualité du produit et la sécurité des patients/consommateurs. Il ne suffit pas de simplement embaucher des personnes ; une formation continue et la vérification de leurs connaissances sont essentielles.
Éléments clés à vérifier et considérations :
- Formation initiale : Tout le personnel impliqué dans la fabrication, la transformation, l'emballage, l'étiquetage et le contrôle qualité doit recevoir une formation initiale approfondie couvrant les bases des BPF, les SOP pertinentes et les pratiques d'hygiène. Cette formation doit comprendre des démonstrations pratiques et des évaluations.
- Formation spécifique au rôle : Au-delà d'une sensibilisation générale aux BPF, la formation doit être adaptée aux fonctions et responsabilités spécifiques de chaque poste. Un analyste du contrôle qualité requiert des connaissances différentes de celles d'un opérateur de production.
- La documentation est primordiale : Conserve des registres méticuleux de toute la formation, incluant les dates, les sujets abordés, les résultats des évaluations et les signatures du personnel. Ces registres fournissent une preuve de conformité et peuvent être cruciaux lors des audits.
- Évaluation des compétences : Ne faites pas que...livrerformationvérifierCompréhension. Mettre en œuvre des évaluations régulières des compétences (examens écrits, démonstrations pratiques, observations) pour s'assurer que le personnel est capable d'appliquer efficacement ses connaissances.
- Formation de recyclage : Les BPF sont en constante évolution et les processus changent. Des formations de recyclage régulières permettent aux employés de se tenir informés des nouvelles réglementations, procédures et bonnes pratiques. La fréquence dépend du poste et des exigences changeantes.
- Hygiène et pratiques personnelles : Renforcez l'importance de l'hygiène personnelle et des pratiques de travail sécuritaires. Cela comprend le lavage des mains, l'utilisation appropriée des équipements de protection individuelle (EPI) et le signalement de toute préoccupation liée à la santé pouvant avoir un impact sur la sécurité des produits.
- Formation des entrepreneurs : N'oubliez pas les contractuels ou le personnel temporaire ! Ils doivent recevoir une formation BPF appropriée, pertinente par rapport à leurs missions, souvent similaire à celle dispensée aux employés permanents.
- Conservation des archives : Établir des procédures claires pour la conservation des registres de formation pendant la durée requise, conformément aux directives réglementaires.
Une équipe bien formée est votre première ligne de défense contre les problèmes de qualité - investissez dans leur développement et assurez-vous qu'elle possède les connaissances et les compétences nécessaires pour produire de manière constante des produits sûrs et efficaces.
Installations et équipements - Maintenir un environnement contrôlé
Un système GMP robuste repose sur l'intégrité de vos installations et la fiabilité de vos équipements. Cela va bien au-delà du simple fait de disposer d'un espace propre ; il s'agit de créer et de maintenir un environnement contrôlé qui minimise les risques de contamination, de croisée de contamination et d'erreurs.
Considérations relatives aux installations :
La conception et l'agencement de votre établissement jouent un rôle essentiel. Veuillez prendre en compte les points suivants :
- Accès contrôlé : Limitez l'accès aux zones de fabrication au personnel autorisé uniquement. Mettez en place des mesures de sécurité rigoureuses et des protocoles pour les visiteurs.
- Ventilation et gestion de l'air appropriées : Assurer une ventilation et des systèmes de filtration de l'air adéquats pour minimiser les contaminants en suspension dans l'air. Surveiller et entretenir régulièrement ces systèmes, y compris les filtres HEPA lorsque cela s'applique.
- Séparation des activités : Définir et séparer clairement les différentes zones en fonction du risque, telles que le stockage des matières premières, la transformation, l'emballage et la mise en quarantaine. Empêcher la contamination croisée entre ces zones.
- Lutte antiparasitaire : Mettez en place un programme complet de lutte antiparasitaire pour prévenir les infestations. Cela comprend des inspections régulières, la mise en place de pièges et des mesures préventives. Documentez méticuleusement toutes les activités.
- Matériaux de surface : Utilisez des matériaux durables, ne perdant pas de fibres, facilement nettoyables et résistants aux produits chimiques utilisés dans vos processus. Évitez les matériaux poreux autant que possible.
- Éclairage : Un éclairage adéquat et approprié est essentiel pour la visibilité et la sécurité des opérateurs.
Intégrité des équipements :
L'efficacité de votre équipement dépend de son entretien. Une approche proactive de la gestion de l'équipement est essentielle.
- Planning de maintenance préventive : Établir et respecter scrupuleusement les calendriers de maintenance préventive pour tout l'équipement critique. Documenter toutes les activités de maintenance.
- Calibrage et Validation : Calibrer et valider régulièrement l'équipement afin d'assurer la précision et la fiabilité. Conserver des registres détaillés de ces activités.
- Conception et matériaux des équipements : Sélectionner l'équipement fabriqué à partir de matériaux compatibles avec les produits et les agents nettoyants utilisés.
- Nettoyage et désinfection : Élaborer et valider des procédures de nettoyage et de désinfection rigoureuses pour tout l'équipement. Documenter ces procédures et vérifier leur efficacité.
- Qualification des équipements : Vérifiez que tout nouvel équipement est correctement validé avant utilisation, en confirmant qu'il fonctionne comme prévu et répond à toutes les exigences. Cela inclut la Qualification d'Installation (QI), la Qualification Opérationnelle (QO) et la Qualification de Performance (QP).
- Gestion des modifications pour les équipements : Toute modification ou réparation d'équipement doit être gérée avec soin par le biais d'un système de contrôle des changements afin de garantir qu'elle ne compromette pas la qualité du produit ni la validation des processus.
Documentation et archivage - Garantir la traçabilité
Une documentation rigoureuse ne se limite pas à cocher des cases ; elle constitue le socle d'un système GMP conforme et efficace. Chaque étape, de la réception des matières premières à la mise en libération du produit fini, doit être enregistrée de manière méticuleuse et être facilement accessible. Considérez votre documentation comme le récit détaillé du parcours de votre produit - un récit que chacun, y compris les auditeurs, doit pouvoir comprendre.
Pourquoi est-ce si important ?Traçabilité. En cas de rappel, d'enquête ou de problème de qualité, des enregistrements complets et précis vous permettent d'identifier rapidement l'origine du problème, d'évaluer son impact et de mettre en œuvre des actions correctives. Sans cela, vous naviguez à l'aveugle.
Qu'est-ce qui doit être documenté ? La liste est exhaustive, mais les domaines clés comprennent :
- Procédures Opératoires Normalisées (PON) Instructions détaillées pour tous les processus, examinées et approuvées régulièrement.
- Dossiers de lots : Dossiers complets de chaque lot de production, incluant les matières premières utilisées, les réglages des équipements, les actions de l'opérateur et les résultats des tests.
- Dossiers de calibration et d'entretien des équipements : Preuve du bon fonctionnement et du respect des spécifications techniques.
- Dossiers de formation : Documentation de la formation des employés, attestant de leurs compétences dans leurs fonctions.
- Rapports de déviation : Constat de toute déviation par rapport aux procédures établies, comprenant les conclusions de l'enquête et les mesures correctives.
- Dossiers de gestion des modifications : Documentation de toute modification apportée aux processus, aux équipements ou aux matériaux, comprenant les études d'impact et les autorisations.
Principes clés pour une tenue de dossiers efficace :
- Précision : Vérifiez que les données soient exactes, complètes et lisibles.
- Ordre chronologiqueLes enregistrements doivent être conservés par ordre chronologique.
- Dossiers originaux : Conserver les documents originaux (ou copies certifiées).
- Accès contrôlé : Limitez l'accès aux dossiers au personnel autorisé.
- Stockage sécurisé : Conservez les archives dans un environnement sûr et à température et humidité contrôlées.
- Examen régulier : Vérifiez régulièrement les dossiers afin de garantir leur exactitude et leur exhaustivité.
- Dossiers électroniques : Si vous utilisez des enregistrements électroniques, assurez-vous que les systèmes sont validés et conformes aux réglementations applicables (par exemple, la 21 CFR Part 11 pour les produits pharmaceutiques aux États-Unis).
Matières premières et composants - Qualité dès le départ
L'adage selon lequel on ne peut pas faire une bourse de soie à partir d'une oreille de cochon s'applique également à la fabrication. La qualité de votre produit fini est intrinsèquement liée à la qualité des matières premières et des composants utilisés pour le créer. Un programme de gestion des matières premières performant n'est pas seulement une exigence réglementaire, mais un élément fondamental d'un système de qualité réussi.
Cette section se concentre sur la mise en place de contrôles garantissant que seuls des matériaux appropriés entrent dans votre processus de fabrication. Cela va au-delà d'une simple commande auprès d'un fournisseur ; cela englobe l'ensemble du cycle de vie d'un composant, de l'approvisionnement initial à son utilisation.
Éléments clés d'un programme de contrôle des matières premières et des composants :
- Qualification des fournisseurs : Ne choisissez pas un fournisseur uniquement sur la base du prix. Mettez en place un processus de qualification rigoureux, incluant des audits (annoncés et inopinés), l'examen de leurs systèmes de qualité et la vérification de leur conformité aux réglementations applicables. Cela établit la confiance et la responsabilisation.
- Inspection et Essais entrants : Chaque lot de matériaux entrants doit subir une inspection et des tests, conformément aux spécifications établies. Cela comprend des vérifications visuelles, des tests analytiques (par exemple, pureté, identité, dosage) et, potentiellement, une évaluation sensorielle selon le matériau. Des plans d'échantillonnage clairement définis sont essentiels.
- Identification et traçabilité des matériaux : Mettez en place un système permettant d'identifier et de remonter chaque lot de matière première jusqu'à son fournisseur et à la documentation associée de manière claire et précise. Les numéros de lot uniques, le scan de codes-barres et les systèmes de suivi électronique sont des outils précieux.
- Quarantine et libération : Les matières entrantes doivent être mises en quarantaine jusqu'à ce qu'elles aient été inspectées, testées et autorisées pour utilisation. Une procédure de libération claire, documentée par du personnel autorisé, empêche l'utilisation accidentelle de matières non conformes.
- Conditions de stockage : Des conditions de stockage appropriées sont essentielles au maintien de l'intégrité du matériau. Contrôlez la température, l'humidité, l'exposition à la lumière et les autres facteurs environnementaux selon les spécifications indiquées dans la fiche technique du matériau.
- État du matériel et durée de conservation : Suivre l'état des matières (p. ex. en quarantaine, approuvées, périmées) et gérer méticuleusement les dates de péremption. Les principes du premier entré, premier sorti (PEPS) doivent être strictement appliqués.
- Gestion des non-conformités : Mettre en place une procédure claire pour la gestion des matériaux non conformes, comprenant la documentation, l'investigation et la mise en quarantaine. Les matériaux rejetés doivent être retournés au fournisseur ou éliminés de manière appropriée.
En mettant en œuvre ces contrôles, vous établissez une base solide pour la qualité et minimisez le risque de défauts de produits résultant de matières premières de qualité inférieure.
Contrôles des processus de fabrication - Exécution cohérente
Les contrôles du processus de fabrication sont la pierre angulaire d'une production de qualité. Ce n'est pas suffisant pour...avoirprocessus validés ; vous devez les exécuter de manière constante. Cela signifie vous assurer que chaque lot, chaque étape, est réalisée conformément aux procédures établies, et que toute déviation est identifiée et traitée sans délai.
Considérez cela comme une recette : même la meilleure recette est inutile si les ingrédients ne sont pas mesurés correctement ou si le temps de cuisson est faux. De même, des procédures opérationnelles standard (POS) robustes ne sont efficaces que si elles sont suivies avec rigueur.
Éléments clés pour une exécution cohérente :
- Tests en cours : Surveillez régulièrement les paramètres critiques (température, pH, viscosité, etc.) tout au long du processus de fabrication. Mettez en œuvre un calendrier clair pour les tests et assurez-vous que les résultats sont enregistrés et évalués avec précision.
- Dossiers de lots : Ce sont les récits détaillés de votre processus de fabrication. Ils doivent documentertout- des numéros de lot de matières premières aux réglages des équipements et aux initiales des opérateurs. Des enregistrements de lots précis et complets sont essentiels pour la traçabilité et les enquêtes.
- Formation et compétence des opérateurs : Le personnel effectuant les étapes de fabrication doit être correctement formé et faire preuve de compétence dans ces tâches. Ce n'est pas un événement ponctuel ; une formation continue et des mises à jour sont essentielles.
- Étalonnage et maintenance des équipements : Un équipement correctement étalonné et entretenu offre des performances fiables et reproductibles, réduisant ainsi la variabilité de votre processus.
- Gestion des écartsToute déviation par rapport aux procédures établies doit être documentée, examinée et résolue rapidement. Cela permet d'identifier les problèmes potentiels et de prévenir leur réapparition.
- Surveillance en temps réel (si applicable) : La mise en place de systèmes de surveillance en temps réel peut fournir des alertes immédiates en cas d'écarts et permettre de prendre des mesures correctives de manière proactive. Ceci est particulièrement précieux pour les processus particulièrement sensibles.
La cohérence ne consiste pas seulement à suivre des règles, mais à intégrer la qualité à chaque étape de votre processus de fabrication.
Gestion des écarts et CAPA - Tirer les leçons des erreurs
Les écarts - ces déviations imprévues par rapport aux procédures établies - sont inévitables dans tout processus de fabrication. L'important n'est pas de les éliminer complètement (un objectif irréaliste !), mais de mettre en place un système robuste pour les identifier, les étudier et les résoudre. C'est là que la gestion des écarts et les actions correctives et préventives (CAPA) entrent en jeu. Considérez cela comme une boucle d'apprentissage : une erreur se produit, vous comprenez pourquoi elle s'est produite, vous la corrigez et vous l'empêchez de se reproduire.
Un système de gestion des écarts bien structuré comprend des procédures de reporting claires, garantissant que tout écart - aussi mineur soit-il - est documenté immédiatement. Ce rapport doit enregistrer des détails tels que la date, l'heure, la description de l'écart, le personnel impliqué et l'action corrective immédiate prise. Ne négligez pas les écarts mineurs ; ils peuvent être des signes avant-coureurs de problèmes systémiques plus importants.
La phase d'investigation est cruciale. Elle nécessite une analyse approfondie des causes profondes afin de déterminerpourquoiL'écart s'est produit. Il ne suffit pas de simplement traiter le symptôme ; il faut comprendre la cause sous-jacente. S'agissait-il d'un problème de formation, d'un équipement défectueux, d'une lacune dans les procédures, ou d'autre chose ? L'utilisation de techniques comme la méthode des 5 Pourquoi peut être extrêmement utile pour creuser le sujet.
Une fois la cause profonde identifiée, l'action corrective vise à résoudre ce problème spécifique. Les actions préventives, quant à elles, sont des mesures proactives prises pour éviter que des écarts similaires ne se reproduisent à l'avenir. Les deux types d'actions doivent être clairement documentés, mis en œuvre et suivis.
Il est crucial de vérifier l'efficacité des actions correctives et préventives. Ces actions ont-elles réellement résolu le problème et empêché sa réapparition ? L'examen régulier des données de déviation et de l'efficacité des actions correctives et préventives (CAPA) est essentiel pour l'amélioration continue de votre système de qualité. Un système CAPA performant transforme les déviations en opportunités précieuses d'apprentissage et de croissance.
Gestion des modifications - Piloter efficacement les changements
Les changements sont inévitables dans tout environnement de fabrication. Qu'il s'agisse d'un ajustement d'un processus, d'une mise à niveau d'un équipement ou d'une modification des matières premières, les modifications peuvent avoir un impact sur la qualité et la sécurité des produits. C'est là qu'un système de gestion des changements robuste devient absolument essentiel. Il ne s'agit pas seulement de procéder à des changements, mais de les gérer.efficacementafin de minimiser les risques et de maintenir la conformité.
Un processus de gestion des modifications bien défini garantit que toute modification proposée subit une évaluation approfondie avant sa mise en œuvre. Cette évaluation doit prendre en compte l'impact potentiel sur la qualité du produit, la validation des processus, la qualification des équipements et la documentation. Il s'agit d'une approche multidimensionnelle qui implique l'avis de différents services - production, assurance qualité, ingénierie, et potentiellement d'autres - afin de fournir une vision globale de la modification.
Les éléments clés d'un système de gestion du changement efficace comprennent :
- Demande de modification : Un système formel de soumission des modifications proposées, précisant clairement la justification, la portée et l'impact prévisible.
- Évaluation d'impact : Une analyse détaillée de la manière dont ce changement affectera divers aspects du processus de fabrication, notamment la qualité, la sécurité et la conformité réglementaire.
- Évaluation des risques : Identifier et évaluer les risques potentiels liés au changement, et élaborer des stratégies d'atténuation.
- Flux de validation : Un processus documenté de révision et d'approbation des modifications, impliquant du personnel désigné disposant de l'autorité et de l'expertise nécessaires pour prendre des décisions éclairées.
- Mise en œuvre et validation : Exécution soignée du changement, suivie d'une validation ou d'une revérification afin de garantir qu'il n'affecte pas la qualité du produit.
- Documentation et archivage : Documentation complète du processus de gestion des changements, incluant la demande initiale, l'évaluation de l'impact, l'évaluation des risques, la documentation d'approbation et les résultats de la validation.
Ne pas mettre en place un système de gestion du changement robuste peut entraîner des erreurs coûteuses, des rappels de produits, un examen réglementaire et nuire à la réputation de votre entreprise. Il s'agit d'un investissement préventif pour maintenir l'intégrité de vos opérations de fabrication et témoigner de votre engagement envers la qualité et la conformité.
Mise en œuvre et révision : passer à l'action avec votre liste de contrôle
La création d'une liste de contrôle GMP n'est qu'une première étape. La véritable valeur réside dans l'application constante de...en utilisantet veiller à ce qu'il reste efficace. Voici comment intégrer avec succès votre liste de contrôle dans vos opérations quotidiennes et la maintenir alignée sur les exigences en constante évolution.
Attribuer la propriété et la formation : Ne laissez pas votre liste de contrôle devenir un document oublié. Attribuez clairement la responsabilité de chaque élément de la liste de contrôle. Des individus ou des équipes doivent être tenus responsables de l'exécution des vérifications, de la documentation des résultats et de l'escalade de tout problème. Il est crucial de fournir une formation complète sur la manière d'exécuter correctement chaque élément de la liste de contrôle et de comprendre les principes GMP sous-jacents. Une formation de remise à niveau régulière est essentielle.
Intégrer au flux de travail : La liste de contrôle ne doit pas s'avérer une charge supplémentaire. Intégrez-la de manière transparente dans les flux de travail existants. Cela pourrait impliquer d'intégrer les éléments de la liste de contrôle dans les procédures opérationnelles standard (POS), d'utiliser des applications de listes de contrôle numériques, ou de la lier aux enregistrements de lots. Réfléchissez à la manière de minimiser les perturbations tout en maximisant l'efficacité.
Adoptez les solutions numériques : Bien que les listes de contrôle papier aient leur utilité, les solutions numériques offrent des avantages considérables. Elles peuvent automatiser la collecte de données, faciliter les rapports en temps réel, améliorer la précision des données et simplifier les pistes d'audit. Explorez des options telles que les listes de contrôle sur tablette, les plateformes basées sur le cloud et les systèmes de tenue de registres électroniques.
Examens et vérifications réguliers : Votre liste de contrôle GMP n'est pas un document statique. Planifiez des examens réguliers - au moins annuellement, et idéalement plus fréquemment - pour garantir sa pertinence continue. Réalisez des audits internes pour vérifier le respect de la liste de contrôle et identifier les axes d'amélioration. Comparez les résultats par rapport aux périodes précédentes afin de suivre les performances et de détecter les tendances.
5. Examen par la direction et amélioration continue : L'examen régulier des données relatives à la performance des listes de contrôle est essentiel. Cela offre un espace de discussion des résultats, de priorisation des mesures correctives et de mise à jour des listes de contrôle en fonction des leçons tirées. Favorisez une culture d'amélioration continue où les commentaires de tous les niveaux de l'organisation sont les bienvenus et pris en compte. N'oubliez pas que les BPF sont un parcours, et non une destination.
Ressources et liens
- FDA Biopharmaceutical CGMP Q&A : Official FDA guidance documents and frequently asked questions related to current Good Manufacturing Practices (cGMP) for biopharmaceutical products. A crucial resource for understanding regulatory expectations.
- ISO 211 - Pharmaceutical GxP Auditing : Provides a framework for auditing pharmaceutical quality systems and is frequently referenced when discussing GMP. Useful for understanding auditing standards.
- United States Pharmacopeia (USP) : Provides standards for pharmaceutical ingredients, excipients, and dosage forms. Relevant for ensuring quality and consistency in raw materials and finished products.
- American Society for Quality (ASQ) : A professional organization dedicated to quality. Provides resources, training, and publications related to quality management, including GMP principles.
- Pharmaceutical Online : Industry news, articles, and resources covering pharmaceutical manufacturing, quality, and regulatory compliance. Provides insights into current trends and best practices.
- GMP Compliance : Provides news, resources, and training focused specifically on GMP compliance. Offers practical advice and regulatory updates.
- ComplianceWorld : Offers a range of compliance resources, including articles, webinars, and training materials covering GMP and other regulated industries. Useful for keeping up with regulatory changes.
- EMC2 : Specializes in regulatory compliance software and services, including solutions for managing GMP documentation and training. Useful for understanding technology-driven solutions.
- MasterControl : Offers quality management system (QMS) software that often incorporates GMP compliance features. Provides insights into digital implementation of GMP processes.
- NSF International : Provides certification and testing services related to food, water, and pharmaceutical products. Relevant for ensuring compliance with specific standards and quality requirements.
- Centers for Disease Control and Prevention (CDC) : While broader, the CDC website can provide valuable information on contamination control, hygiene, and sanitation - critical aspects of maintaining a controlled facility environment.
Questions fréquemment posées
Que signifie l'acronyme GMP et pourquoi est-il important ?
Les BPF sont les Bonnes Pratiques de Fabrication. Il s’agit d’un système garantissant que les produits sont fabriqués et contrôlés de manière cohérente, conformément aux normes de qualité. Elles sont essentielles pour des secteurs tels que la pharmacie, l’alimentation et la cosmétique, afin de protéger la sécurité des consommateurs et l'efficacité des produits.
Qui doit utiliser une liste de contrôle GMP ?
Toute entreprise impliquée dans la fabrication de produits réglementés par une autorité (comme la FDA aux États-Unis) devrait utiliser une liste de contrôle GMP. Cela inclut les fabricants, les fournisseurs et les distributeurs.
Quels types de produits sont généralement couverts par les réglementations GMP ?
Les réglementations GMP couvrent souvent les produits pharmaceutiques, les produits biologiques, les dispositifs médicaux, les produits alimentaires, les compléments alimentaires, les cosmétiques et les principes actifs pharmaceutiques (API).
Que contient généralement un modèle de liste de contrôle GMP ?
Une liste de contrôle GMP complète comprend généralement des sections sur la formation du personnel, la validation des équipements, la maintenance des installations, le contrôle des documents, le contrôle qualité, la manipulation des matières premières et la gestion des déviations.
Puis-je modifier le modèle de liste de contrôle GMP fourni dans l'article ?
Oui, le modèle est conçu pour être personnalisé. Vous devriez l'adapter à vos processus, produits et exigences réglementaires spécifiques. Examinez et mettez à jour régulièrement votre liste de contrôle pour tenir compte de toute modification.
Quelle est la différence entre une liste de contrôle GMP et une procédure opératoire normalisée (PON) ?
Une liste de contrôle GMP est un document utilisé pour vérifier que les SOP sont respectés. Les SOP, quant à eux, détaillent précisément *comment* une tâche spécifique doit être effectuée. Une liste de contrôle confirme le respect des SOP.
À quelle fréquence un document de contrôle GMP devrait-il être examiné et mis à jour ?
Les listes de contrôle GMP doivent être examinées et mises à jour au moins une fois par an, ou plus fréquemment si des changements importants sont apportés aux procédés, aux réglementations ou aux conclusions d'audits.
Que se passe-t-il si un audit BPF révèle des problèmes de non-conformité ?
Des manquements peuvent entraîner des lettres de mise en garde, des rappels de produits, des alertes aux importations, voire des poursuites judiciaires. Il est crucial de traiter les constats rapidement avec des actions correctives et préventives (CAPA).
Où puis-je trouver plus d'informations sur les réglementations GMP ?
Vous trouverez des informations détaillées sur les réglementations BPF sur les sites web des organismes de réglementation tels que la FDA (États-Unis), l’EMA (Europe) et d’autres spécifiques à votre région et à votre secteur.
Comment savoir si ma liste de contrôle GMP est réellement efficace ?
Une liste de contrôle efficace est régulièrement utilisée, mise à jour en fonction des constats d'audit et des modifications des processus, et témoigne d'une conformité constante aux exigences des BPF. Des audits internes périodiques peuvent aider à évaluer son efficacité.
Cet article vous a-t-il été utile ?
Démonstration de la solution de gestion de la production
Arrêtez de vous battre avec les paperasses et les systèmes fragmentés ! Notre solution apporte clarté et contrôle à votre processus de production. Des procédures opérationnelles standard (POS) et de la maintenance des équipements au contrôle qualité et au suivi des stocks, nous simplifions chaque étape.
Articles connexes
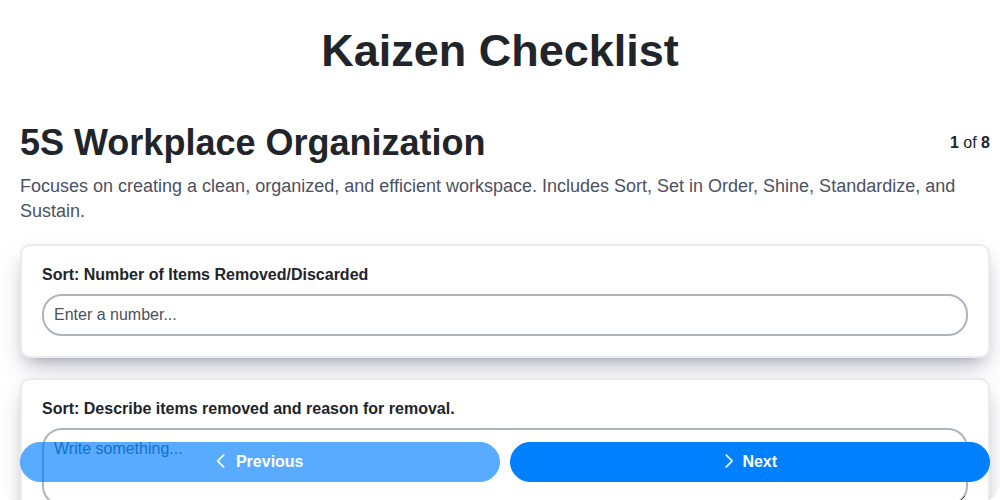
Modèle de liste de contrôle Kaizen : Votre parcours vers l’amélioration continue.

Machine Safety Audit Checklist: Your Guide to a Safer Manufacturing Workplace
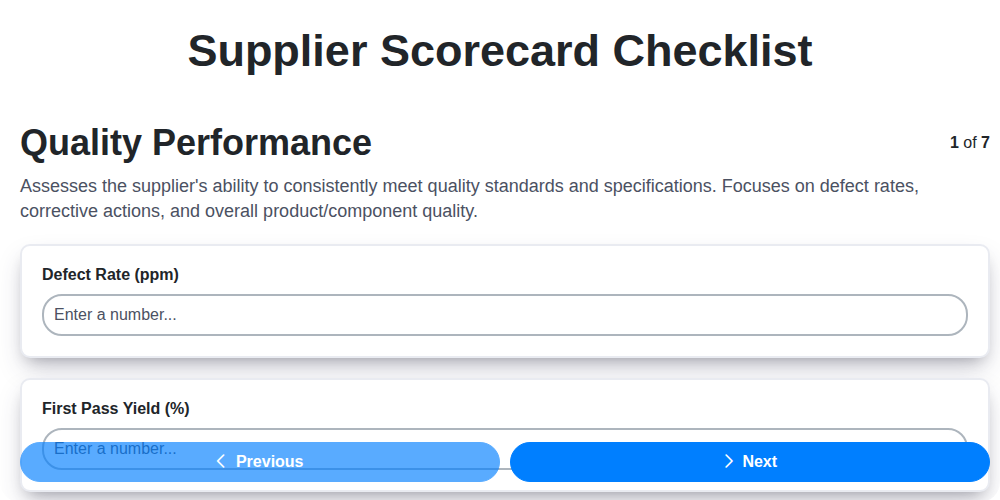
Mastering Supplier Performance: Your Free Supplier Scorecard Checklist Template
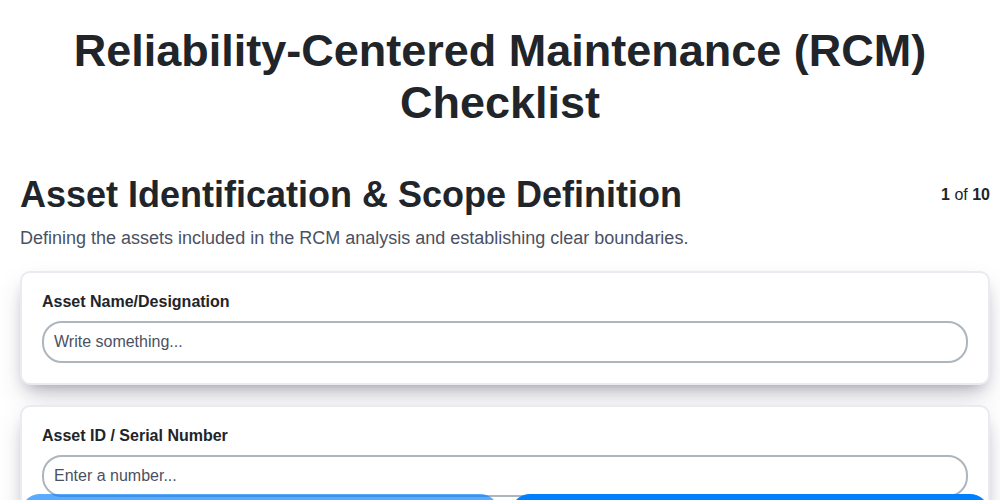
Votre modèle ultime de liste de contrôle RCM : Un guide étape par étape

Modèle de liste de contrôle LPA : Votre guide pour les audits de processus structurés

Votre modèle de liste de contrôle LOTO ultime

Your Ultimate FSC 22000 Checklist Template
Modèle de liste de contrôle d'inspection qualité : Prévenir les défauts et améliorer les processus de fabrication
Nous pouvons le faire ensemble
Besoin d'aide avec les listes de contrôle?
Vous avez une question ? Nous sommes là pour vous aider. Veuillez soumettre votre demande et nous vous répondrons rapidement.