Вашът основен шаблон за проверка (GLP): Практическо ръководство
Публикувано: 09/01/2025 Обновено: 03/19/2026
Съдържание
- Въведение: Защо е важен списък за проверка на ГЛП.
- Разбиране на основните принципи на GLP
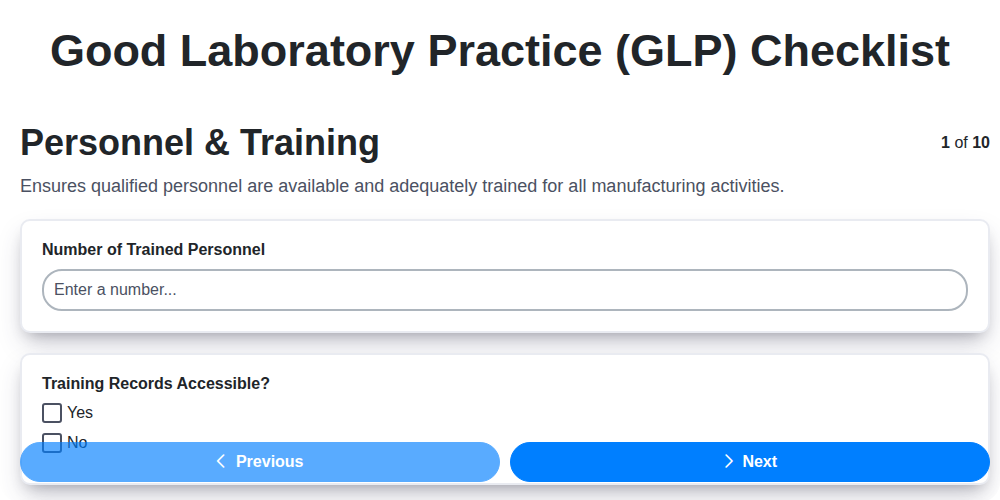
- Раздел 1: Персонал и обучение - Изграждане на квалифициран екип
- Раздел 2: Съоръжения и Оборудване - Осигуряване на Контролирана Среда
- Раздел 3: Управление на материалите - Поддържане на проследимост
- Раздел 4: СОП-ове и процедури - Основата на последователността
- Раздел 5: Цялост на данните и водене на записи: Критичен фокус
- Глава 6: Контрол на качеството и тестване - Проверка на резултатите Ви
- Глава 7: Отстраняване на отклонения и разследвания - Учене от грешките
- Глава 8: Контрол на промените: Ефективно управление на модификациите
- Раздел 9: Квалификация и валидиране на оборудването - Доказателство за ефективност
- Раздел 10: Валидиране на процеса: Осигуряване на възпроизводимост
- Прилагане на вашия шаблон за контролен списък за добра лабораторна практика
- Ресурси и връзки
Съкратено: Трябва ли да осигурите, че вашата лаборатория отговаря на стандартите за добра лабораторна практика (ДЛП)? Този наръчник предоставя практичен шаблон за контролен списък, покриващ всичко - от обучение на персонала и поддръжка на помещенията до управление и валидиране на данни. Изтеглете го, адаптирайте го към вашите процеси и го използвайте, за да проследявате систематично съответствието и да поддържате интегритета на данните!
Въведение: Защо е важен списък за проверка на ГЛП.
В света на научните изследвания и продуктовото развитие, цялостта на данните не е просто желателна черта - тя е основата на доверието и съответствието с изискванията. Насоките за добра лабораторна практика (GLP) са създадени, за да гарантират, че генерираните данни са надеждни, проследими и защитими. Но знаейки...принципиСпазването на GLP е само половината от битката. Последователното прилагане, щателното водене на документация и бдителността към детайлите са от решаващо значение за постигане на истинско съответствие с GLP. Именно тук добре структурираният списък за проверка на GLP става безценен инструмент. Той е повече от просто списък със задачи - предоставя ясна пътна карта за вашата лаборатория, насърчавайки култура на отчетност и минимизирайки риска от скъпоструващи грешки или регулаторни провали. Представете си го като гаранция на вашата лаборатория, че всеки процес, всяко наблюдение и всеки резултат са документирани, валидирани и, в крайна сметка, надеждни.
Разбиране на основните принципи на GLP
GLP не е просто списък с правила; това е философия, изградена върху няколко основни принципа. В основата й стои непоколебимата отдаденост на целостта на данните - осигуряване на точност, надеждност и проследимост на данните. Това надхвърля простото записване на наблюдения; то изисква щателно внимание към детайлите, спазване на утвърдени процедури и система от проверки и противотежести.
Няколко основни принципа стоят в основата на тази ангажираност. ПланиранеТова е от първостепенна важност. Добре дефиниран протокол, очертаващ целите на изследването, методологията и статистическия анализ, е основата.Представление отнася се до последователната реализация на протокола от обучен персонал.Документация е крайъгълен камък на GLP - всяко действие, наблюдение и изчисление трябва да бъде записано ясно и своевременно.Осигуряване на качество (ОК)е независимият орган, който проверява съответствието с GLP, действайки като ключова гаранция срещу грешки и неспазване. Накрая,Архивиранегарантира дългосрочно запазване и достъпност на данните за одити и бъдещи справки. Признаването и спазването на тези принципи е основата за генериране на надеждни научни данни и постигане на истинско съответствие с GLP.
Раздел 1: Персонал и обучение - Изграждане на квалифициран екип
Успехът на една лаборатория зависи от експертизата и компетентността на нейния персонал. Съответствието с GLP не е само въпрос на процедури и оборудване; то е фундаментално свързано с наличието на квалифициран екип, който разполага с необходимите знания и умения, за да изпълнява задълженията си точно и етично. Това започва с внимателен подбор и продължава с непрекъснато обучение и оценка на работата.
Отвъд дипломите: Оценка на компетентността
Въпреки че формалното образование и опитът са важни, задълбочена оценка на практически умения е от решаващо значение. Ръководителите по подбор на персонал трябва да отдават приоритет на кандидати, които демонстрират задълбочено разбиране на принципите на добра лабораторна практика (GLP) и ангажираност към запазване на целостта на данните. Тази оценка може да включва практически демонстрации, интервюта, базирани на сценарии, и оценки на умения за решаване на проблеми. Обмислете оценки на умения, съобразени със специфичните изисквания на длъжността.
Обучителният път: От въвеждане до непрекъснато развитие
Първоначалното обучителен процес трябва да обхване основните принципи на GLP, специфичните SOP-та, свързани с ролята на служителя, и основните протоколи за безопасност. Това трябва да включва преглед на очакванията за интегритет на данните и значението на точното водене на записи. Записи за обучение.трябвада се поддържа старателно, с документация за обхванатото съдържание, датите на обучение и имената на обучителите и обучаваните.
Непрекъснато развитие - Ангажимент за усъвършенстване.
Обучението не трябва да бъде еднократно събитие. Една стабилна програма включва редовни курсове за повторение, актуализации относно промени в нормативната уредба и обучение за нови технологии или методологии. Обмислете включването на възможности за кръстосано обучение с цел да се разширят уменията на персонала и да се подобри гъвкавостта. Оценките на работата трябва да включват проверка за спазване на добрите лабораторни практики и да идентифицират области за професионално развитие. Културата на непрекъснато учене дава сили на вашия екип да поддържа най-високите стандарти за качество и съответствие.
Раздел 2: Съоръжения и Оборудване - Осигуряване на Контролирана Среда
Основата на надеждните данни започва с щателно контролирана среда. Съоръженията и оборудването играят ключова роля за поддържането на целостта на данните, а проактивният подход към тяхното управление е от първостепенно значение. Това не е просто въпрос на чистота; става въпрос за осигуряване на контролирани условия, които минимизират променливостта и потенциалните източници на грешки.
Здравият раздел "Съоръжения и Оборудване" във вашия контролен списък за ДБП трябва да обхване няколко ключови области. На първо място, обмислете физическото разположение. Има ли достатъчно пространство за извършване на всички необходими процедури безопасно и ефективно? Отделянето на несъвместими материали е от съществено значение - предотвратяването на случайно замърсяване е критична превантивна мярка. Вентилационните системи трябва да бъдат обект на редовни проверки и поддръжка, за да се осигури добро качество на въздуха и отстраняване на потенциално вредни изпарения.
Контролът на температурата и влажността често е от съществено значение, особено за чувствителни проби или реактиви. Документираните програми за мониторинг на околната среда, включително редовно регистриране и калибриране на сензори за температура и влажност, са от критично значение.
Преминавайки към оборудването, е необходим системен подход. Всяка част от оборудването, използвано в дейности, свързани с GLP, трябва да се поддържа и калибрира правилно съгласно документиран график. Записи на тези дейности, включително дати, резултати и участващ персонал, са от съществено значение. Освен рутинната поддръжка, трябва да се извършват и документират квалификация при инсталиране (IQ), оперативна квалификация (OQ) и квалификация на производителността (PQ) за критично оборудване, за да се гарантира, че е инсталирано правилно, функционира според предназначението си и работи последователно. Накрая, трябва да има система за управление на несъответстващо оборудване - такова, което е извън експлоатация или изисква ремонт - за да се предотврати неговата неоторизирана употреба.
Раздел 3: Управление на материалите - Поддържане на проследимост
Ефективното управление на материалите е крайъгълен камък за съответствие с GLP, оказващо пряко влияние върху цялостта и възпроизводимостта на данните. Това не е просто съхранение на химикали, а създаване на одитируем запис за всеки материал, използван във вашите изследвания. Това означава щателна документация от момента, в който даден материал влезе в лабораторията, до неговото изхвърляне или използване в краен продукт.
Ключови елементи на проследимостта:
- Изчерпателни записи на инвентарните данни: Системата за управление на складовите наличности е от съществено значение. Тя трябва да включва данни като информация за доставчици, номера на партиди, дата на получаване, срок на годност, получено количество и местоположение в лабораторията. Настоятелно се препоръчват дигитални системи за ефективност и точност.
- Уникална идентификация: Всеки контейнер с материал трябва да бъде уникално идентифициран, обикновено чрез етикет. Етикетите трябва да включват наименованието на материала, концентрацията, партиден номер, дата на отваряне и инициалите на лицето, което го е отворило.
- Контролиран достъп: Ограничете достъпа до складови помещения само до оторизиран персонал. Това свежда до минимум риска от неразрешено използване или замърсяване.
- Запазени проби: Запазете представителни мостри от всяка партида материал, използвана в GLP проучвания. Тези мостри трябва да бъдат надлежно етикетирани и съхранявани, и тяхната цялост трябва да бъде поддържана. Те са жизненоважни за бъдещи справки, повторни изследвания или разследвания.
- Регистър за използване на материали: Поддържайте подробни регистри, документиращи употребата на всеки материал в конкретни изследвания или експерименти. Тези регистри трябва да включват датата, количеството използвано, номера на изследването и инициалите на лицето, използващо материала.
- Редовни одити: Провеждайте редовни одити на системата за управление на материалите, за да идентифицирате и коригирате всякакви несъответствия или слабости. Това включва проверка на точността на записите, правилното съхранение на материалите и наблюдение на сроковете на годност.
Ефективното управление на ресурсите не е просто процедурна необходимост; то е жизненоважен гарант, който защитава целостта на вашите данни и достоверността на вашето изследване.
Раздел 4: СОП-ове и процедури - Основата на последователността
Стандартните оперативни процедури (СОП) не са просто документация; те са основата за възпроизводими резултати и свидетелство за ангажимента на вашата лаборатория към качеството. Разглеждайте ги като споделена памет на вашата лаборатория, документиращакакЗадачите се изпълняват последователно, всеки път. Без стабилни стандартни оперативни процедури, започват да се промъкват отклонения, данните стават ненадеждни, а спазването на изискванията се превръща в постоянен труден процес.
Ефективните SOP-та надхвърлят обикновените стъпка по стъпка инструкции. Те трябва ясно да определят целта на процедурата, да идентифицират отговорните лица, да посочват необходимото оборудване и материали, да очертават предпазните мерки и да описват очакваните резултати. Те не са статични документи; те се нуждаят от редовен преглед и актуализации, за да отразяват промени в процесите, технологиите или регулаторните изисквания.
Критично е, стандартните оперативни процедури (СОП) са толкова добри, колкото обучението, което ги придружава. Проверката на разбирането, чрез практически демонстрации или оценки, е от съществено значение, за да се гарантира, че целият персонал следва процедурите правилно. Редовните одити за спазване на СОП са също така жизненоважни за идентифициране на области за подобрение и за затвърждаване на култура на съответствие. Една добре поддържана и активно използвана програма за СОП не е просто за отбелязване на изпълнени задачи - тя е за изграждане на основа от научна строгост и цялостност на данните.
Раздел 5: Цялост на данните и водене на записи: Критичен фокус
Цялостта на данните е крайъгълен камък на спазването на добрите лабораторни практики (GLP), а воденето на надеждни записи е нейното практическо въплъщение. Не става въпрос просто за документиране на случилото се, а за осигуряване на точност, пълнота, последователност, трайност и достъпност на тези записи. Компрометирана цялост на данните може да доведе до сериозни последици, от регулаторни санкции до обезсмислени резултати от изследвания.
Този раздел се фокусира върху основните практики за поддържане на цялостността на данните и щателното водене на документация.
- Оригиналните данни са от първостепенно значение.Всички необработени данни, генерирани по време на GLP проучване - независимо дали става въпрос за разпечатки от уреди, ръкописни бележки или електронни записи - трябвабъдете оригиналният запис. Това означава, че не трябва да има презапис, изтриване или промяна на данните. Ако са необходими корекции, те трябва да бъдат направени с датиран, подписан допълнителен документ, който ясно да се позовава на първоначалния запис.
- Одитни следи за електронни записи: При използване на електронни системи, уверете се, че са активирани и функционират коректно подробни регистри за одит. Тези регистри трябва да проследяват всяко действие, предприето в системата, включително въвеждане на данни, модификации и изтривания. Редовно преглеждайте логовете на регистрите за одит, за да идентифицирате всякакви аномалии.
- Сигурно съхранение на данни и контрол на достъпа: Внедрете надеждни контролни механизми за достъп, за да ограничите достъпа до данни само за оторизиран персонал. Използвайте сигурни методи за съхранение (както физически, така и електронни), за да защитите данните от загуба, кражба или неоторизирана модификация.
- Политики за съхранение на данни: Създайте ясни политики за съхранение на данни, които да отговарят на законовите изисквания и вътрешните правила на организацията. Тези политики трябва да определят за какъв период от време записите трябва да се съхраняват и как трябва да бъдат архивирани.
- Ясна маркировка и индексиране: Уверете се, че всички записи са ясно обозначени и индексирани, за да се улесни лесното им извличане и проследимост. Това е особено важно за физическите записи.
- Хронологичен редПоддържайте записите в стриктен хронологичен ред, за да осигурите точно представяне на хода на изследването.
- Обучение и информираност: Обучавайте редовно персонала относно принципите за цялост на данните и най-добрите практики за водене на документация. Културата на осведоменост е от ключово значение за предотвратяване на неволни грешки.
Глава 6: Контрол на качеството и тестване - Проверка на резултатите Ви
Контролът на качеството (КК) и тестването са основните стълбове за надеждни данни във всяка лаборатория, отговаряща на изискванията на GLP. Не е достатъчно просто да...изпълнявам тестове; трябва задълбочено да проверите дали тези тестове са точни, прецизни и последователно дават надеждни резултати. Тази секция разглежда ключови съображения за надеждни процедури за контрол на качеството и тестване.
Валидиране на методите: Основата на доверието
Преди да бъде използвана каквато и да е аналитична методика за изследвания, свързани с ДБП, тотрябвада бъде валидиран. Валидирането демонстрира, че методът е подходящ за предназначението си. Това обикновено включва оценка на параметри като:
- Прецизност: Колко близо е резултатът от теста до реалната стойност.
- Прецизност: Повторяемостта и възпроизводимостта на резултатите. (Разглеждайте повторяемостта - в рамките на едно изследване, и възпроизводимостта - при различни анализатори, уреди и дни).
- Специфичност/ИзбирателностСпособността на метода да измерва само целевия аналит, без смущения.
- Граница на откриване (ГО): Най-ниската концентрация на аналит, която може да бъде засечена.
- Долен праг на количествено определяне (ДПКО): Най-ниската концентрация на аналит, която може надеждно да бъде определена количествено.
- ЛинейностОбхватът, в който методът дава пропорционални резултати.
- Устойчивост: Способността на метода да удържа малки промени в условията (например температура, pH).
Процесите на валидиране са щателно документирани, а критериите за приемане са ясно дефинирани.преди Започва тестване. Отклоненията от тези критерии трябва да бъдат проучени и отстранени, преди методът да може да бъде сметнат за валидиран.
Непрекъснат контрол на качеството - Отвъд първоначалната проверка
Валидирането не е еднократно събитие. Непрекъснатият контрол на качеството (QC) е от съществено значение за поддържане на целостта на данните. Това включва:
- Контролни проби: Извършвайте контролни изследвания с проби с известни концентрации заедно с изследваните проби, за да следите работата на аналитичната система. Те трябва да бъдат представителни за матрицата и аналитите, които се изследват.
- Криви на калибриране: Редовно генериране и валидиране на калибрационни криви с помощта на стандартни разтвори с известни концентрации.
- Поддръжка на оборудването: Въвеждане на график за превантивна поддръжка на цялото аналитично оборудване, за да се гарантира неговата правилна функционалност.
- Управление на реагенти и стандартни образци: Строг контрол върху съхранението, обработката и сроковете на годност на реагенти и стандарти.
- Преглед на данните: Подробен преглед на всички сурови данни и резултати с цел идентифициране на всякакви аномалии или тенденции, които могат да подсказват проблем.
Чрез поставяне на приоритет на строги процедури за контрол на качеството и тестване, изграждате основа от увереност в данните си, осигурявайки съответствие и повишавайки достоверността на вашите изследователски резултати.
Глава 7: Отстраняване на отклонения и разследвания - Учене от грешките
Отклоненията са неизбежна част от всяка лабораторна работа. Те представляват случаи, в които процедурите не са били следвани точно според инструкциите в СОП-овете, възникнали са неочаквани резултати или апаратурата е отказвала. Въпреки това, самото съществуване на отклонение не е повод за безпокойство; то е...обработкана тази отклонение, което наистина има значение. Една стабилна процедура за обработка на отклонения не е за търсене на виновници, а за идентифициране на възможности за подобрение и предотвратяване на повторение.
Структуриран подход към справянето с отклонения трябва да включва няколко ключови стъпки. Първо,откриване и документиранеТе са от първостепенно значение. Всички отклонения, независимо от видимата им тежест, трябва незабавно да бъдат документирани. Тази документация трябва да включва ясно описание на случилото се, кога се е случило, кои са били замесени и потенциалното въздействие върху целостта на данните.
След това, задълбоченоразследване трябва да бъде инициирано. Това надхвърля простото отбелязване на отклонението; изисква потапяне вкоренна причинаБеше ли проблем с обучението? Дефектна стандартна оперативна процедура? Неизправност на оборудването? Системен проблем в процеса? Използването на инструменти като техниката Пет Защо може да бъде безценно за разкриване на корена на проблема.
След като бъде установена първопричината,коригиращи и превантивни мерки (КПМ) Трябва да се разработи и приложи план. Корективните мерки трябва да решат непосредствения проблем, за да се предотврати неговото повторение в бъдеще.същотоСитуацията. Превантивните мерки са насочени към отстраняване на първопричината, за да се предотвратят подобни проблеми в бъдеще.другобласти на лабораторията.
Критично е целият процес за обработка на отклонения да бъде документиран щателно. Това включва първоначалния доклад за отклонение, резултатите от разследването, плана за коригиращи и превантивни действия (CAPA) и потвърждението, че коригиращите и превантивни действия са били ефективни. Тази документация служи като ценна следа за одити и демонстрира ангажимент към непрекъснато подобрение. Не забравяйте, отклонението не е провал; то е възможност за учене - шанс да укрепите процесите във вашата лаборатория и да повишите надеждността на вашите данни.
Глава 8: Контрол на промените: Ефективно управление на модификациите
Промените са неизбежни във всяка лабораторна среда. Независимо дали става въпрос за актуализация на стандартна оперативна процедура, ново оборудване или промяна в протокол за изследване, ефективното управление на тези промени е от първостепенно значение за поддържане на съответствие с добрите лабораторни практики (GLP) и целостта на данните. Надеждна система за контрол на промените гарантира, че всякакви изменения се оценяват щателно, документират се и се прилагат по контролиран начин, като се минимизират потенциалните рискове и се запазва надеждността на вашите данни.
Основният елемент на успешна система за контрол на промените е документирана процедура. Тази процедура трябва да очертава стъпките за иницииране на заявка за промяна, извършване на оценка на риска за разбиране на потенциалното въздействие, получаване на необходимите одобрения, внедряване на промяната и проверка на нейната ефективност. Критично важно е да се определи кой има правомощия да инициира, преглежда и одобрява промени.
Не всички промени изискват еднакво ниво на проверка. Вашата система трябва да категоризира промените въз основа на техния потенциален риск - малък, умерен и голям - и да определя съответните нива на преглед и изисквания за документация. Например, незначителна печатна грешка в стандартна оперативна процедура може да изисква проста одобряване и документация, докато значителна промяна в производствен процес би наложила цялостно валидационно проучване.
Отвъд самата промяна, помислете за верижните реакции. Промените в една област често могат да засегнат и други. Вашата оценка на риска трябва проактивно да идентифицира тези потенциални ефекти като верижна реакция и да включва стратегии за смекчаване. Правилното обучение също е от съществено значение; персоналът трябва да бъде информиран за промените и да разбира как те засягат неговите роли и отговорности. Накрая, не забравяйте редовно да преглеждате самата процедура за контрол на промените, за да гарантирате нейната ефективност и актуалност по отношение на развиващите се лабораторни операции.
Раздел 9: Квалификация и валидиране на оборудването - Доказателство за ефективност
Квалификацията и валидирането на оборудването не са просто отмятане на пунктове; те са за осезаемо доказателство, че вашето оборудване последователно функционира според предназначението си и дава надеждни данни. Това е многопластов процес, създаден да вдъхне увереност във всеки експеримент и резултат.
Процесът на квалификация обикновено включва три ключови етапа:
- Квалификация на инсталацията (КИ): Това удостоверява, че оборудването е монтирано правилно, съгласно спецификациите на производителя, и е свързано коректно към комунални услуги като електричество, вода и газ. Документацията включва серийни номера, дати на монтаж и информация за доставчика.
- Оперативна квалификация (ОК): Този етап демонстрира, че оборудването функционира според спецификациите на производителя при определени работни условия. Това често включва тестване на производителността в широк диапазон от параметри. Критериите за приемане са предварително определени и трябва да бъдат изпълнени.
- Квалификация на работата (КВ) Това е финалната стъпка, потвърждаваща, че оборудването последователно отговаря на утвърдените критерии за приемане при използване за предназначената му цел в конкретната лабораторна среда. По същество това валидира, че работата на оборудването е надеждна и повтаряема.
Валидацията се простира отвъд оборудването. Аналитичните методи, софтуерът, използван за придобиване и анализ на данни, и дори цели процеси изискват валидиране, за да се гарантира тяхната точност, надеждност и съответствие с изискванията за Добра лабораторна практика (ДЛП). Това включва документирани доказателства, че методът/софтуерът/процесът последователно дава очакваните резултати, когато се използва съгласно предварително определени процедури.
Критично е документацията за квалификация и валидация да се поддържа щателно, да е леснодостъпна и да се преглежда периодично, за да се гарантира непрекъснато съответствие. Всички отклонения или неизпълнения трябва да бъдат щателно проучени и документирани, с прилагане и проверка на коригиращи действия. Целта не е просто еднократно квалифициране и валидиране, а създаване на система за непрекъснати гаранции и непрекъснато подобрение.
Раздел 10: Валидиране на процеса: Осигуряване на възпроизводимост
Валидацията на процесите не е просто желателна, а е основен елемент от Добра лабораторна практика (ДЛП) и критична демонстрация на вашата способност последователно да произвеждате надеждни данни или продукти. Тя надхвърля простото следване на процедура - става въпрос за доказване, че процесът...винагиФункционира според очакванията при определени условия. Това обикновено включва демонстриране на това, че процесът постоянно работи в рамките на предварително определени критерии за приемане.
Има три основни етапа на валидиране на процес: Проектиране на валидиране на процеси,Квалификация на процесаиНепрекъсната верификация на процесите (НВП) .
- Проектиране и валидиране на процеси: Този етап се фокусира върху потвърждаването на това, че проектът на процеса е устойчив и способен да постигне желаните резултати. Често това се постига чрез задълбочени оценки на риска, симулации и пилотни изследвания. Този етап определя базовата линия за вашия процес и очакваното му представяне.
- Квалификация на процеса: След като проектът бъде валидиран, квалификацията на процеса потвърждава, че той работи последователно, когато се изпълнява в реални работни условия. Това включва изпълнение на множество валидационни цикли при внимателно контролирани параметри, щателно документиране на резултатите и доказване, че са изпълнени всички критерии за приемливост.
- Непрекъсната верификация на процесите (НВП)CPV е текуща оценка на валидирания процес. Включва периодичен мониторинг на критични параметри на процеса (КПП) и критични качествени характеристики (ККХ), за да се осигури постоянен контрол на процеса и да се идентифицират евентуални отклонения, които изискват разследване. Диаграми за статистически контрол на процесите (ДСП) често се използват в CPV за проследяване на тенденциите в процеса и за задействане на сигнали при необходимост.
Надеждното процесно валидиране демонстрира ангажираността ви към запазване на целостта на данните, намалява риска от продуктови дефекти и укрепва позицията ви по отношение на регулаторното съответствие. Подробната документация през целия жизнен цикъл на валидирането е от първостепенно значение за готовност при одити и проследимост.
Прилагане на вашия шаблон за контролен списък за добра лабораторна практика
Статичен контролен списък, колкото и изчерпателен да е, е само началото. Истинското спазване на добрите лабораторни практики (GLP) изисква динамичен и проактивен подход. Ето как да надхвърлите документа и активно да интегрирате контролния списък в ежедневните операции:
Определете отговорност и отчетност: Не позволявайте на списъка с проверки да се събира прах. Възложете на конкретни хора или екипи отговорност за всяка секция. Това гарантира, че някой активно следи, обновява и разрешава идентифицираните проблеми. Ясната отговорност насърчава чувството за отчетност и стимулира непрекъснато подобрение.
Интегриране в работните процеси: Интегрирайте безпроблемно елементите от списъците за проверка в съществуващите работни процеси в лабораторията. Не ги третирайте като допълнителен елемент; направете ги неразделна част от начина, по който се изпълняват задачите. Например, включете стъпки за проверка от списъка в SOP-тата или използвайте дигитални списъци, интегрирани с LIMS (Системи за управление на лабораторна информация).
Внедрете редовни цикли за преглед. Задайте редовни цикли на преглед (седмични, месечни, тримесечни), за да оценявате систематично спазването на контролния списък. Тези прегледи не трябва да бъдат наказателни; те са възможности за учене, идентифициране на затруднения в процесите и укрепване на добрите лабораторни практики.
Използвайте дигитални инструменти: Приемете технологията! Дигиталните шаблони за контролни списъци, интегрирани с анализ на данни, могат да автоматизират напомняния, да проследяват представянето и незабавно да подчертават области, изискващи внимание. Това надхвърля ръчните процеси и предоставя информация в реално време.
Насърчаване на култура на открита комуникация: Насърчете членовете на екипа да идентифицират и докладват проактивно всякакви отклонения или притеснения. Важна е култура без упреци; фокусирайте се върху извличането на поуки от грешките и подобряването на процесите. Направете списъка с проверки инструмент за колективен растеж, а не източник на безпокойство.
Проследяване на тенденции и анализ на данни: Не просто отмятайте квадратчета; анализирайте данните! Идентифицирайте повтарящи се проблеми, следете показателите за ефективност и използвайте тази информация, за да стимулирате подобрения в процесите и да усъвършенствате вашата програма за добра лабораторна практика. Статичен документ се превръща в динамичен инструмент за непрекъснато усъвършенстване на качеството.
Ресурси и връзки
- U.S. Food and Drug Administration (FDA) : The FDA is the primary regulatory body overseeing GLP compliance in the US. Their website provides regulations, guidance documents, and information related to GLP.
- U.S. Environmental Protection Agency (EPA) : The EPA also regulates GLP, particularly related to environmental testing. Their site offers relevant guidance and resources.
- Organisation for Economic Co-operation and Development (OECD) : The OECD provides internationally harmonized GLP principles. This is a key resource for understanding the global perspective on GLP.
- United States Pharmacopeia (USP) : USP provides standards and resources related to quality assurance and control, which are highly relevant to GLP implementation. While not solely focused on GLP, their materials offer valuable insights.
- Pharmaceutical and Medical Devices Agency (PMDA) - Japan : Provides information and guidelines related to GLP as implemented in Japan. Offers a different regional perspective on GLP regulations.
- International Organization for Standardization (ISO) : ISO provides standards and guidelines applicable to quality management systems, many of which align with GLP principles. ISO 9001, in particular, is relevant.
- ASTM International : ASTM develops and publishes voluntary consensus standards used globally. While not exclusively GLP focused, their standards often cover aspects like equipment calibration and validation, which are crucial for GLP compliance.
- NiceQuest : Provides GLP training courses and resources. A commercial offering, but often provides a good overview of GLP principles and requirements.
- ComplianceBridge : Offers GLP consulting, training, and software solutions. Provides practical guidance and support for GLP implementation.
- Global GMP : A resource offering news, regulatory updates, and training related to GMP and GLP. Provides a broad perspective on compliance.
- QSA, Inc. : Provides GLP audits and consulting services. They offer valuable insights into common GLP deficiencies and best practices.
- EMC2 Group : Consulting firm specializing in regulatory compliance, including GLP. Offers training and auditing services.
- SPS Compliance : Provides GLP consulting, auditing, and training services. Focused on helping companies achieve and maintain GLP compliance.
Често Задавани Въпроси
Какво означава съкращението GLP и защо е важно?
GLP означава Добри лабораторни практики. Това е система за управление на качеството, предназначена да гарантира надеждността и интегритета на неклинични лабораторни изследвания, особено тези, които подкрепят регулаторни подавания (като например за лекарства или пестициди). Спазването на принципите на GLP гарантира, че данните са точни, проследими и надеждни.
Кой трябва да използва списък за проверка на GLP?
Всеки, участващ в провеждането или управлението на неклинни лабораторни изследвания, които трябва да спазват изискванията на GLP. Това включва ръководители на лаборатории, ръководители на изследвания, изследователски персонал, специалисти по управление на данни и служители, отговарящи за осигуряване на качеството.
Какво включва шаблона ви за контролен списък за ДПП?
Нашият шаблон обхваща ключови области от съответствието с Добрите лабораторни практики (ДЛП), включително поддръжка на помещенията и оборудването, стандартни оперативни процедури (СОП), обучение на персонала, управление на данните, провеждане на изследвания и дейности за осигуряване на качеството. Проектиран е да бъде адаптивен към различни типове изследвания и организационни нужди.
Този шаблон за списък може ли да се персонализира?
Да! Шаблонът е предназначен да бъде отправна точка. Лесно можете да добавяте, премахвате или променяте елементи, за да го адаптирате към вашите специфични протоколи за изследвания, стандартни оперативни процедури и регулаторни изисквания. Насърчаваме потребителите да го персонализират, за да отговаря най-добре на техните нужди.
В какъв файлов формат е налична шаблона за контролен списък?
Шаблонът за контролен списък е предоставен във формат Microsoft Excel (.xlsx), което позволява лесно редактиране, проследяване и въвеждане на данни.
Как да използвам шаблона за контролен списък ефективно?
1. Прегледайте елементите от контролния списък и разберете основните принципи на ДБХ. 2. Персонализирайте контролния списък, за да отговаря на специфичните протоколи на вашето проучване и СОП. 3. Използвайте го по време на планирането, провеждането и приключването на проучването. 4. Документирайте всички предприети действия и всички отклонения от контролния списък. 5. Редовно преглеждайте и обновявайте контролния списък, за да осигурите неговата продължаваща ефективност.
Каква е ролята на ръководител на изследвания във връзка със списъка за проверка на ДОП?
Директорът на изследването е крайно отговорен за осигуряване на съответствие с GLP. Той/тя трябва активно да участва в процеса на контролен списък, да преглежда попълнените списъци и да отстранява всякакви установени недостатъци. Контролният списък е ценен инструмент за директора на изследването, за да следи съответствието и да поддържа целостта на данните.
Какво ще се случи, ако открия несъответствие, използвайки контролния списък?
Откритите недостатъци трябва да бъдат документирани, проучени и отстранени. Трябва да бъде разработен и приложен план за коригиращи действия, за да се предотврати повторение. Документацията на контролния списък трябва ясно да очертава недостатъка, предприетите коригиращи действия и потвърждението за ефективност.
Може ли този контролен списък да се използва за проучвания, които не са пряко свързани с нормативни документи?
Въпреки че е разработен с оглед на съответствие с нормативните изисквания, списъкът може да бъде адаптиран за използване във всяко лабораторно изследване, където са от съществено значение качествени данни и проследимост, дори и да не се представя директно на регулаторни органи.
Тази статия беше полезна?
Демонстрация на решение за управление на производството
Спрете да се занимавате с документация и да се борите с несвързани системи! Нашето решение осигурява яснота и контрол върху производствения ви процес. От стандартни оперативни процедури (СОП) и поддръжка на оборудване до контрол на качеството и проследяване на инвентара, ние опростяваме всяка стъпка.
Свързани статии
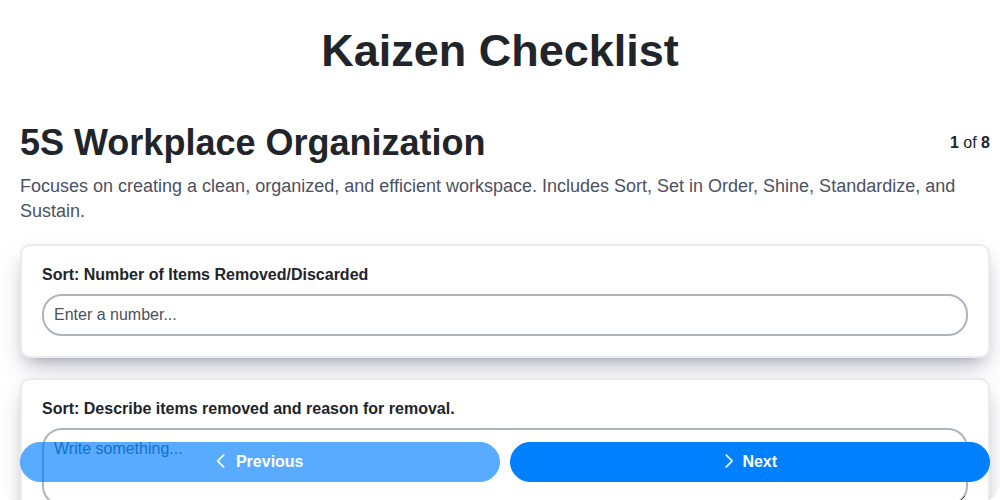
Шаблон за контролна листа Кайдзен: Вашият път към постоянно подобрение

Machine Safety Audit Checklist: Your Guide to a Safer Manufacturing Workplace
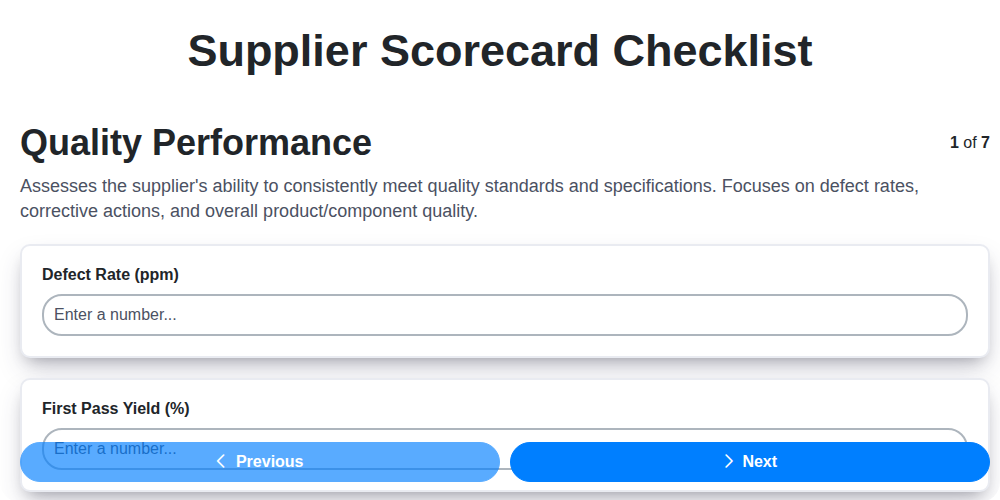
Mastering Supplier Performance: Your Free Supplier Scorecard Checklist Template
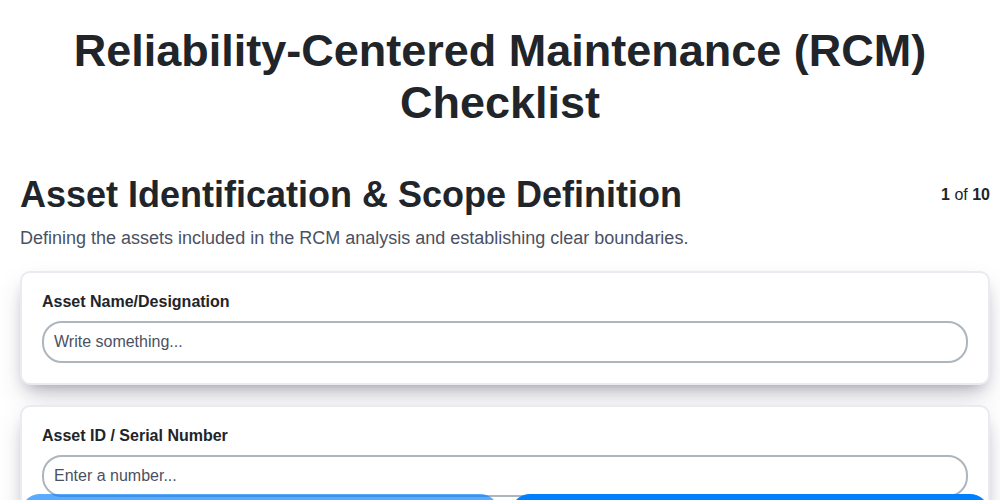
Your Ultimate RCM Checklist Template: A Step-by-Step Guide

Шаблон за контролен списък LPA: Вашето ръководство за слоести одити на процеси

Вашият краен шаблон за контролен списък за заключване/етикетиране (ЛОТО)

Your Ultimate FSC 22000 Checklist Template
Шаблон за проверка на качеството: Предотвратяване на дефекти и подобряване на производствените процеси
Можем да го направим заедно
Нуждаете се от помощ с
Производство?
Имате въпрос? Тук сме, за да помогнем. Моля, изпратете запитването си и ние ще отговорим своевременно.