Вашата необходима проверка (чеклист) по GMP шаблони: Пътеводител стъпка по стъпка
Публикувано: 09/02/2025 Обновено: 04/10/2026
Съдържание
- Разбиране на основите: Какво е проверка (чеклист) за GMP? (И защо имате нужда от такава)
- Дефиниране на обхвата - Персонализиране на контролния списък според вашите операции
- Персонал и обучение - Изграждане на квалифициран екип
- Съоръжения и оборудване - Поддържане на контролирана среда
- Документация и поддържане на записи - Осигуряване на проследимост
- Суровини и компоненти - Качество от самото начало
- Контрол на производствените процеси - Последователно изпълнение
- Управление на отклонения и CAPA - Учене от грешки
- Управление на промените - Ефективно управление на модификации
- Въвеждане на Вашия контролен списък в действие: Имплементация и преглед
- Ресурси и връзки
Накратко: Получете безплатен, персонализируем чеклист шаблон GMP, за да гарантирате, че производствените ви процеси отговарят на изискванията за качество. Този ръководство ви показва какво покрива всеки раздел - от обучение на персонала до контрол на промените - така че лесно да го адаптирате към вашата специфична индустрия и да останете в съответствие!
Разбиране на основите: Какво е проверка (чеклист) за GMP? (И защо имате нужда от такава)
Проверка за GMP не е просто документ; това е практически израз на ангажимента Ви към качеството и спазването на регулациите. Мислете за нея като структурирано, стъпка по стъпка ръководство, което гарантира, че всеки критичен процес в производството Ви се изпълнява последователно в съответствие с установените процедури и регулаторни изисквания.
В основата си, контролен списък за GMP детайлизира конкретни действия, проверки и записи, необходими във всяка стъпка от производствен процеса - от приемане на суровини до пускане на финалните продукти. Тези елементи не са произволни; те са внимателно избрани, за да адресират потенциални рискове и да осигурят безопасността, ефикасността и консистентността на продукта.
Защо това е толкова важно? Защото регулациите на GMP, въпреки че са всеобхватни, могат да бъдат претоварващи. Списъкът за проверка превръща тези често сложни изисквания в практически стъпки, минимизира вероятността от човешка грешка, насърчава проследяемостта и предоставя конкретно доказателство за спазването на най-добрите практики. Това е повече от просто отбелязване на полета; това е проактивна мярка, която изгражда култура на качество в цялата ви организация.
Дефиниране на обхвата - Персонализиране на контролния списък според вашите операции
Общ контролен списък GMP, макар и добро начало, рядко е достатъчен сам по себе си. Истинската сила е в персонализацията му - съпоставянето му точно с вашите специфични операции и регулаторни задължения. Преди да започнете да запълвате полета, направете пълен инвентар на своите процеси.
Започнете с очертаване на всяка стъпка, включена в производствения си цикъл - от приемане на суровини до освобождаване на крайния продукт. Идентифицирайте критичните точки на контрол (КТК) в всяка стъпка; това са точките, където отклоненията могат значително да повлияят на качеството и безопасността на продукта. Не пренебрегвайте изглежда маловажните процеси - дори административните задачи могат да бъдат от ключово значение.
Вземете предвид регулаторната рамка. Кои GMP насоки са приложими за вашата индустрия и продуктите, които произвеждате? (например, 21 CFR Част 210 и 211 за американските фармацевтични продукти, насоки на ЕС GMP, BRCGS за храните). Тези регулации предписват специфични изисквания, които трябва да бъдат адресирани в вашата контролна листа.
Накрая, помислете за уникалните характеристики на вашата компания - какви оборудвания използвате, какъв е мащабът на вашите операции и какви е специфични рискове, свързани с вашите процеси. Вашият контролен списък трябва да отразява тези елементи, за да осигури наистина ефективно и релевантно ръководство за съответствие с GMP. Това първоначално очертаване ще заложи основата за надежден и персонализиран контролен списък за GMP, който наистина защитава вашия бизнес и вашите клиенти.
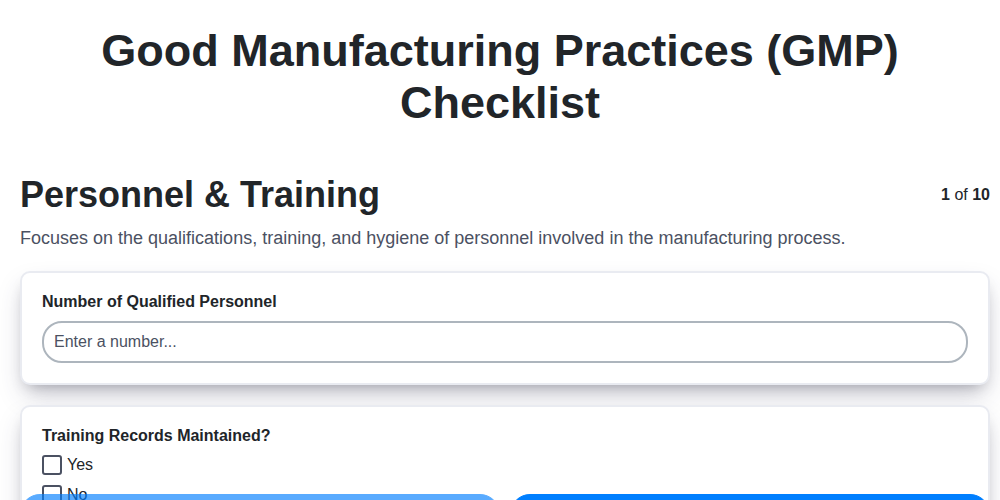
Персонал и обучение - Изграждане на квалифициран екип
Системата за добро производство (GMP) изисква си персонал, който е добре обучен и компетентен. Ходовият персонал е гръбнакът на всяка производствена дейност, и разбирането им на принципите на GMP пряко влияе върху качеството на продукта и безопасността на пациента/потребителя. Не е достатъчно просто да наемете хора; непрекъснатото обучение и проверка на техните знания са от критично значение.
Ключови проверки и съображения:
- Първоначално обучение: Вероятният персонал, пряко зает с производството, обработката, опаковането, етикетирането и контрола на качеството, трябва да премине пълно начално обучение, което да обхваща основите на GMP, съответните работни процедури (SOP) и хигиенични практики. Това трябва да включва и практически демонстрации и преценки.
- Обучение по роли: Повъд общата осведоменост относно GMP, обучението трябва да бъде адаптирано към конкретните длъжности и отговорности. Анализатор на контрол на качеството изисква различно знание от оператора в производството.
- Документацията е изключително важна: Поддържайте детайлна документация за всички обучения, включително дати, покрити теми, резултати от оценки и подписи на персонала. Тези записи предоставят доказателство за спазване на изискванията и могат да бъдат от ключово значение по време на одити.
- Оценка на компетентностите: Не самода доставяобучение;проверетеИзграждане на разбиране. Внедрявайте регулярни оценки на компетентностите (пишени изпити, практически демонстрации, наблюдение), за да се гарантира, че персонала могат ефективно да прилагат знанията си.
- Преговорно обучение: GMP се развива постоянно и процесите се променят. Планираното допълнително обучение поддържа служителите актуални относно новите регулации, процедури и най-добри практики. Честотата зависи от длъжността и променящите се изисквания.
- Хигиена и лична обмислие: Подчертайте важността на личната хигиена и безопасните работни практики. Това включва миене на ръце, правилно използване на индивидуални средства за защита (ИЗЗ) и докладване на всякакви здравословни проблеми, които могат да повлияят на безопасността на продукта.
- Обучение на изпълнител: Не забравяйте и външни изпълнители или временен персонал! Те трябва да получат подходящо обучение по GMP, свързано с техните задачи, което често отговаря на обучението, предоставяно на постоянните служители.
- Съхраняване на записи: Установете ясни процедури за съхранение на записи на обучение за изискваната продължителност, както изискват регулаторните насоки.
Добро обучен екип е вашата първа линия на защита срещу проблеми с качеството - инвестирайте в тяхното развитие и уверете се, че имат знанията и уменията да произвеждат последователно безопасни и ефективни продукти.
Съоръжения и оборудване - Поддържане на контролирана среда
Ефективната система, съгласно Добър производствена практика (GMP), зависи от цялостта на вашите помещения и надеждността на вашето оборудване. Това надхвърля простото поддържане на чисто място; става въпрос за създаване и поддържане на контролирана среда, която минимизира риска от замърсяване, кръстосано замърсяване и грешки.
Изисквания към обекта:
Дизайнът и разположението на вашето помещение играят решаваща роля. Учете тези основни точки:
- Контролиран достъп: Ограничете достъпа до производствените зони само за оторизиран персонал. Внедрете строги мерки за сигурност и протоколи за посетители.
- Правилна вентилация и пречистване на въздуха: Осигурете адекватна вентилация и системи за филтриране на въздуха, за да минимизирате въздушното замърсяване. Редовно проверявайте и поддържайте тези системи, включително HEPA филтри, когато е приложимо.
- Разделяне на дейностите: Ясно дефинирайте и отделите различните зони въз основа на риска, като например съхранение на суровини, обработка, опаковане и карантина. Предотвратете кръговото замърсяване между тези зони.
- Борба с вредители: Въведете цялостна програма за борба с вредителите, за да предотвратите заразе. Това включва рутинни проверки, капанж и превантивни мерки. Документирайте всички дейности с детайлност.
- Повърхностни материали: Използвайте материали, които са издръжливи, не пушат влакна, лесно почистваеми и устойчиви на химикали, използвани в вашите процеси. Избягвайте порести материали по възможност.
- Осветление: Адекваното и подходящо осветление е съществено за видимостта и безопасността на операторите.
Целост на оборудването:
Вашето оборудване е добро само колкото е поддръжката му. Проактивният подход към управлението на оборудването е от първостепенно значение.
- Графици за превантивно обслужване: Установете и стриктно спазвайте графика за превантивно обслужване на цялото критично оборудване. Документирайте всички поддържащи дейности.
- Калибриране и валидиране: Редовно калибрирайте и валидирайте оборудването, за да осигурите точност и надеждност. Поддържайте подробни записи на тези дейности.
- Проектиране и материали на оборудването: Изберете оборудване, изработено от материали, съвместими с продуктите и почистващите средства, които се използват.
- Почистване и дезинфекция: Разработете и валидирайте надеждни процедури за почистване и дезинфекция за цялото оборудване. Документирайте тези процедури и проверете тяхната ефективност.
- Квалификация на оборудването: Уверете се, че всички нови оборудвания са долно квалифицирани преди употреба, като се потвърди, че работят както е предвидено и отговарят на всички изисквания. Това включва квалификация на инсталацията (IQ), квалификация на експлоатацията (OQ) и квалификация на изпълнението (PQ).
- Контрол на промените за оборудване: Всички модификации или ремонти на оборудването трябва да се управляват внимателно чрез система за контрол на промените, за да се гарантира, че не компрометират качеството на продукта или валидирането на процеса.
Документация и поддържане на записи - Осигуряване на проследимост
Надстройките в документацията не са просто за отбелязване на полета; те са гръбначният стълб на съответстваща и ефективна GMP система. Всеки етап, от приемане на суровини до освобождаване на крайния продукт, трябва да бъде изчерпателно документиран и лесно достъпен. Представете си документацията си като подробна история за пътуването на Вашия продукт - история, която всеки, включително одитори, трябва да може да разбере.
Защо е толкова важно?Проследимост. При извикване, разследване или при опасения относно качеството, пълните и точни записи ви позволяват бързо да идентифицирате източника на проблема, да прецените въздействието му и да предприемете корективни действия. Без нея, работите на угатство.
Какво трябва да бъде документирано?Списъкът е изчерпателен, но основните области включват:
- Стандартни работни процедури (СРП): Подробни инструкции за всички процеси, които се преглеждат и одобряват редовно.
- Годишни записи: Пълни записи на всяка партида, включително използвани суровини, настройки на оборудването, действия на операторите и резултати от тестването.
- Протоколи за калибриране и поддръжка на оборудването: Доказателство за правилно функциониране и съответствие на оборудването на спецификациите.
- Протоколи за обучение: Документиране на обучението на служителите, демонстриращо компетентност в техните роли.
- Отстъпчивост на доклади: Протоколи от всички отклонения от установен процедури, включително изводи от разследването и корективни действия.
- Протоколи за промяна на контрола: Документиране на всички промени в процесите, оборудването или материалите, включително оценки на въздействието и одобрения.
Основни принципи за ефективно водене на записи:
- Точност: Уверете се, че данните са точни, пълни и разчитани.
- Хронологичен ред: Записите трябва да се поддържат в хронологичен ред.
- Оригинални записи: Поддържайте оригинални записи (или нотариални копия).
- Контролиран достъп: Ограничете достъпа до записи само до упълномочения персонал.
- Сигурно съхранение: Съхранявайте записи в безопасно и контролирано среда.
- Редовно преглеждане: Периодично преглеждайте записи, за да осигурите точност и пълнота.
- Електронни записи: Ако използвате електронни записи, уверете се, че системите са валидирани и отговарят на съответните регулации (например 21 CFR Част 11 за фармацевтични препарати в САЩ).
Суровини и компоненти - Качество от самото начало
Поговорката, че не можеш да направиш люрек от свино ухо, е вярна и в производството. Качеството на крайния ви продукт е пряко свързано с качеството на суровите материали и компонентите, използвани за неговото създаване. Надеждна програма за управление на сурови материали не е просто регулаторно изискване; тя е основополагащ елемент на успешна система за качество.
Този раздел се фокусира върху установяването на контроли, които гарантират, че в производствения ви процес влизат само подходящи материали. Той надхвърля простото поръчване от доставчик; той обхваща целия жизнен цикъл на компонента, от първоначалното извеждане на източници до консумацията.
Основни елементи на програма за контрол на суровини и компоненти:
- Квалификация на доставчика: Не избирайте доставчик само въз основа на цената. Внедрете строг процес на квалификация, включващ одити (каквоначално и неочаквано), преглед на системите за качество и проверка на тяхното спазване на съответните регулации. Това установява доверие и отговорност.
- Входящ контрол и тестване: Всеки входящ мест материал трябва да бъде преминал през инспекция и тестове, съобразени с установените спецификации. Това включва визуални проверки, аналитични тестове (напр. чистота, идентификация, активност) и потенциално дори сензорна оценка в зависимост от материала. Критично е да има ясно дефинирани планове за вземане на проби.
- Идентификация и проследяемост на материала: Въведете система, която ви позволява ясно да идентифицирате и проследявате всяка партия материал до нейния доставчик и свързаната документация. Уникални номера на партиди, сканиране на баркод и електронни системи за проследяване са ценни инструменти.
- Карантин и освобождане: Входящите материали трябва да бъдат карантинирани докато не бъдат инспектирани, тествани и освободени за употреба. Ясна процедура за освобождаване, документирана от упълномощен персонал, предотвратява случайното използване на несъответстващи материали.
- Условия за съхранение: Правилните условия за съхранение са критични за запазване на целостта на материала. Контролирайте температурата, влажността, излагането на светлина и други екологични фактори, както е посочено в техническата спецификация на материала.
- Състояние на материала и срок на годност: Проследявайте статуса на материала (напр. карантинен, одобрен, изтекъл) и управлявайте срока на годност изключително внимателно. Трябва стриктно да се следват принципите първи дойде, първи изтече (FIFO).
- Управление на несъответствия: Установете ясна процедура за обработка на несъответстващи материали, включваща документация, разследване и сегрегация. Отхвърлените материали трябва да бъдат върнати на доставчика или утилизирани по правилния начин.
Чрез прилагането на тези контроли, ви създавате силна основа за качество и минимизирате риска от дефекти в продукта, произтичащи от отстъпни суровини.
Контрол на производствените процеси - Последователно изпълнение
Контролът на производствения процес е гръбнакът на висококачественото производство. Не е достатъчно простоимамвалидирани процеси; трябва последователно да ги прилагате. Това означава да осигурите, че всяка партия, всяка стъпка се извършва съгласно установените процедури и че всяко отклонение е незабавно идентифицирано и коригирано.
Представете си го като рецепта - дори най-добрата рецепта е безполезна, ако съставките са измерени неправилно или времето за готвене е грешно. Подобно, устойчивите СОП (Стандартни работни процедури) са ефективни само когато се следват прецизно.
Ключови елементи за последователно изпълнение:
- Проверка по процес: Редовно следете критичните параметри (температура, pH, вискозитет и др.) през целия производствен процес. Внедрете ясен график за тестване и уверете се, че резултатите са точно регистрирани и оценявани.
- Партидни записи: Това са подробни хроники на производствен процес. Те трябва да документиратвсичкоОт номера на партии на суровини до настройки на оборудването и инициали на операторите. Точните и пълни протоколи за серии са жизненоважни за проследяемостта и изследванията.
- Обучение и компетентност на операторите: Персоналът, извършващ производствени стъпки, трябва да е адекватно обучен и да демонстрира компетентност в тези задачи. Това не е еднократно събитие; непрекъснатото обучение и допълнителното превъзпитание са от ключово значение.
- Калибриране и поддръжка на оборудването: Правилно калибрираното и поддържаното оборудване осигурява надеждна и повторяема работа, минимизирайки вариативността в процеса ви.
- Управление на отклонения: Всяко отклонение от установените процедури трябва да бъде документирано, изследвано и незабавно разрешено. Това помага за идентифициране на потенциални проблеми и предотвратяване на повторение.
- Мониторинг в реално време (когато е приложимо): Внедряването на системи за мониторинг в реално време може да осигури незабавни предупреждения за отклонения и да позволи предприемане на превантивни корективни действия. Това е особено ценно за високочувствителни процеси.
Последователността не е само спазване на правила; тя е въплътяване на качеството във всеки аспект от производствен процес.
Управление на отклонения и CAPA - Учене от грешки
Отклоненията - тези незапланирани отклонения от установените процедури - са неизбежни във всеки производствен процес. Ключът не е да ги елиминираме изобщо (това е илюзионистична цел!), а да създадем надеждна система за тяхното идентифициране, изследване и разрешаване. Тук влизат в действие Управлението на отклоненията и Коригиращите и превантивни действия (CAPA). Мислете за това като учищна верига: се допуска грешка, разбирате защо се е случила, я поправяте и предотвратявате повторното ѝ възникване.
Добро структурирана система за управление на отклонения включва ясни процедури за докладване, гарантирайки, че всяко отклонение - независимо колко незначително изглежда - е незабавно документирано. Тази документация трябва да уловя подробности като дата, време, описание на отклонението, заето персонал и незаминалата коригираща мярка. Не пренебрегвайте малките отклонения; те могат да бъдат ранни предупредителни знаци за по-големи системни проблеми.
Фазата на изследване е критична. Тя изисква подробно изследване на основната причина, за да се определизащоОтстъпването се е случило. Простото отстраняване на симптома не е достатъчно; трябва да разберете основната причина. Беше ли проблем с обучението, неизправна част от оборудването, пропуск в процедурата или нещо изцяло различно? Използването на инструменти като техниката "5 защо" може да бъде невероятно полезно за по-дълбоко копаене.
След като бъде идентифицирана основната причина, коригиращите действия имат за цел да отговорят на този конкретен проблем. Превантивните действия от друга страна са проактивни стъпки, предприети за предотвратяване възникването на подобни отклонения в бъдеще. И двата вида действия трябва да бъдат ясно документирани, въведени и проследени.
Критично е да се провери ефективността на превантивните и корективните действия. Действията наистина ли са решили проблема и предотвратили повторението? Редовното преглеждане на данните за отклонения и ефективността на СПК е жизненоважно за непрекъснато подобряване на системата за качество. Надеждна система за СПК превръща отклоненията от потенциални закъснения в ценни възможности за учене и растеж.
Управление на промените - Ефективно управление на модификации
Промените са неизбежни във всяка производствена среда. Независимо дали става въпрос за фин настройка на процес, ъпгрейд на оборудване или модификация на суровини, промените могат да повлияят на качеството и безопасността на продукта. Именно тук един надежден системен контрол на промените става абсолютно жизненоважен. Става въпрос не само за извършване на промени, а и за управлението им.ефективноза минимизиране на риска и поддържане на съответствие.
Дефиниран процес за контрол на промените гарантира, че всяка предложена модификация преминава през изчерпателна оценка преди внедряване. Тази оценка трябва да отчита потенциалното въздействие върху качеството на продукта, валидацията на процесите, квалификацията на оборудването и документацията. Това е многостранен подход, който изисква информация от различни отдели - производство, осигуряване на качеството, инженерство и потенциално други - за да предостави цялостен поглед върху промяната.
Основни елементи на силна система за контрол на промени включват:
- Иницииране на заявка за промяна: Формална система за подаване на предложени промени, ясно очертаваща обосновацията, обхвата и очакваното въздействие.
- Оценка на въздействието: Подробен анализ на това как промяната ще повлияе на различни аспекти на производствения процес, включително качество, безопасност и спазване на нормативните изисквания.
- Оценка на рисковете: Идентифициране и оценка на потенциалните рискове, свързани със промяната, и разработване на стратегии за смекчаване.
- Работен поток за одобрение: Документиран процес за преглед и одобрение на промени, включващ назначена документация с правомощие и експертиза за вземане на информирани решения.
- Въвеждане и валидиране: Внимателно изпълнение на промяната, последвано от валидиране или ревалидиране, за да се гарантира, че тя не влияе негативно на качеството на продукта.
- Документация и ведение на записи: Изчерпателна документация на процеса за контрол на промените, включваща първоначалния заявка, оценка на въздействието, оценка на риска, документация за одобрение и резултати от валидацията.
Неспазването на внедряване на надеждна система за контрол на промените може да доведе до скъпи грешки, извикване на продукти от пазара, регулаторно внимание и увреждане на репутацията на вашата компания. Това е проактивна инвестиция в поддържането на цялостта на вашите производствени операции и демонстрация на ангажимент към качеството и спазването на нормативните изисквания.
Въвеждане на Вашия контролен списък в действие: Имплементация и преглед
Създаването на контролен списък съгласно GMP е само половината битка. Истинската стойност се крие в последователнотоизползванеи гарантиране, че остава ефективен. Ето как успешно да интегрирате контролната си проверка в ежедневната си работа и да я поддържате в съответствие с променящите се изисквания.
1. Определяне на собственост и обучение: Не позволявайте списъкът ви за проверки да стане прашен документ. Назначете ясна отговорност за всеки пункт в проверката. Индивидите или екипите трябва да отговарят за извършването на проверките, документирането на резултатите и ескалирането на всякакви проблеми. От ключово значение е да осигурите цялостно обучение за правилно изпълнение на всеки пункт в проверката и разбиране на основните принципи на GMP. Редовното предавателно обучение е жизненоважно.
2. Интегриране в работния процес: Проверката не трябва да се усеща като допълнително натоварване. Интегрирайте я безпроблемно в съществуващите работни процеси. Това може да включва включването на елементите от проверката в стандартните работни процедури (СОП), използването на дигитални приложения за проверки или свързването ѝ с партидни записи. Помислете как да минимизирате прекъсването, като същевременно максимизирате ефективността.
3. Приемете дигиталните решения: Докато хартиените контролни списъци имат своето място, дигиталните решения предлагат значителни предимства. Те могат да автоматизират събирането на данни, да улеснят докладването в реално време, да подобрят точността на данните и да опростят следите от одитиране. Проучете опции като контролни списъци, базирани на таблети, облачни платформи и системи за електронен запис на данни.
4. Редовно преглеждане и одитиране: Вашата проверка по GMP не е статичен документ. Планирайте редовни прегледи - поне годишно, а идеално и по-често - за да гарантирате продължителна релевантност. Провеждайте вътрешни одити, за да потвърдите спазването на проверката и да идентифицирате области за подобрение. Сравнете резултатите с предишни периоди, за да проследявате представянето и да уловирате тенденциите.
5. Преглед от ръководството и непрекъснато подобряване: Преглед от ръководството на данните за изпълнение на контролни списъци е от съществено значение. Това осигурява платформа за обсъждане на откритията, приоритизиране на корективни действия и актуализиране на контролните списъци въз основа на наученото. Насърчавайте култура на непрекъснато подобрение, в която се приветстват и се следват от обратната връзка от всички нива на организацията. Запомнете, че GMP е пътуване, а не дестинация.
Ресурси и връзки
- FDA Biopharmaceutical CGMP Q&A : Official FDA guidance documents and frequently asked questions related to current Good Manufacturing Practices (cGMP) for biopharmaceutical products. A crucial resource for understanding regulatory expectations.
- ISO 211 - Pharmaceutical GxP Auditing : Provides a framework for auditing pharmaceutical quality systems and is frequently referenced when discussing GMP. Useful for understanding auditing standards.
- United States Pharmacopeia (USP) : Provides standards for pharmaceutical ingredients, excipients, and dosage forms. Relevant for ensuring quality and consistency in raw materials and finished products.
- American Society for Quality (ASQ) : A professional organization dedicated to quality. Provides resources, training, and publications related to quality management, including GMP principles.
- Pharmaceutical Online : Industry news, articles, and resources covering pharmaceutical manufacturing, quality, and regulatory compliance. Provides insights into current trends and best practices.
- GMP Compliance : Provides news, resources, and training focused specifically on GMP compliance. Offers practical advice and regulatory updates.
- ComplianceWorld : Offers a range of compliance resources, including articles, webinars, and training materials covering GMP and other regulated industries. Useful for keeping up with regulatory changes.
- EMC2 : Specializes in regulatory compliance software and services, including solutions for managing GMP documentation and training. Useful for understanding technology-driven solutions.
- MasterControl : Offers quality management system (QMS) software that often incorporates GMP compliance features. Provides insights into digital implementation of GMP processes.
- NSF International : Provides certification and testing services related to food, water, and pharmaceutical products. Relevant for ensuring compliance with specific standards and quality requirements.
- Centers for Disease Control and Prevention (CDC) : While broader, the CDC website can provide valuable information on contamination control, hygiene, and sanitation - critical aspects of maintaining a controlled facility environment.
Често Задавани Въпроси
Какво означава GMP и защо е важно?
GMP разкрива съкращението Good Manufacturing Practices (Добри производствени практики). Това е система за гарантиране, че продуктите се произвеждат и контролират последователно съгласно стандартите за качество. Тя е жизненоважна за индустрии като фармацевтиката, храните и козметиката, за да се запази безопасността на потребителите и ефективността на продуктите.
Кой се нуждае от използване на Гएमपी чеклист?
Всяка компания, която участва в производството на продукти, регулирани от надзорно тяло (като FDA в САЩ), трябва да използва контролна листа за GMP. Това включва производители, доставчици и дистрибутори.
Какви видове продукти обикновено са покрити от правилата за GMP?
Регламентите за най-добра практика често покриват фармацевтични продукти, биологични препарати, медицински уреди, храни, диетични добавки, козметика и активни фармацевтични съставки (АФС).
Какво се включва в типичен шаблон за контролен списък на съответствие с GMP?
Изчерпателна проверка по принципите на GMP обикновено включва секции за обучение на персонала, валидация на оборудването, поддръжка на съоръженията, контрол на документацията, контрол на качеството, работа с суровини и управление на отклоненията.
Мога ли да модифицирам шаблон на контролен списък за GMP, предоставен в статията?
Да, шаблонът е създаден за персонализиране. Трябва да го адаптирате към вашите специфични процеси, продукти и регулаторни изисквания. Редовно преглеждайте и актуализирайте проверката си, за да отразявате всякакви промени.
Каква е разликата между контролен списък за GMP и стандартна работна процедура (СОП)?
Проверка на съответствието на GMP е документ, използван за потвърждаване, че се спазват стандартните работни процедури (SOP). SOP-ите от своя страна детайлизират точно *как* трябва да бъде изпълнена определена задача. Проверка на съответствието потвърждава спазването на SOP-то.
Колко често трябва да се преглежда и актуализира контролен списък за GMP?
Проверката на GMP списъците трябва да се преглежда и актуализира поне годишно, или по-често, ако има значителни промени в процесите, нормативните актове или резултатите от одити.
Какво става, ако Гएमपी одита открие проблеми с несъответствия?
Проблеми с несъответствия могат да доведат до предупредителни писма, оттегляне на продукти, импортни предупреждения и дори правни действия. От ключово значение е бързо разрешаване на откритията с коригиращи и превантивни действия (CAPA).
Къде мога да намеря повече информация относно нормативните актове за GMP?
Можете да намерите подробна информация за регулациите по GMP на уебсайтовете на регулаторни органи като FDA (САЩ), EMA (Европа) и други, специфични за вашия регион и индустрия.
Как да знам дали моят контролен списък за GMP е наистина ефективен?
Ефективният контролен списък се използва редовно, се актуализира въз основа на резултатите от одита и промените в процесите и демонстрира последователно спазване на изискванията на GMP. Периодичните вътрешни одити могат да помогнат за оценка на неговата ефективност.
Тази статия беше полезна?
Демонстрация на решение за управление на производството
Спрете да се занимавате с документация и да се борите с несвързани системи! Нашето решение осигурява яснота и контрол върху производствения ви процес. От стандартни оперативни процедури (СОП) и поддръжка на оборудване до контрол на качеството и проследяване на инвентара, ние опростяваме всяка стъпка.
Свързани статии
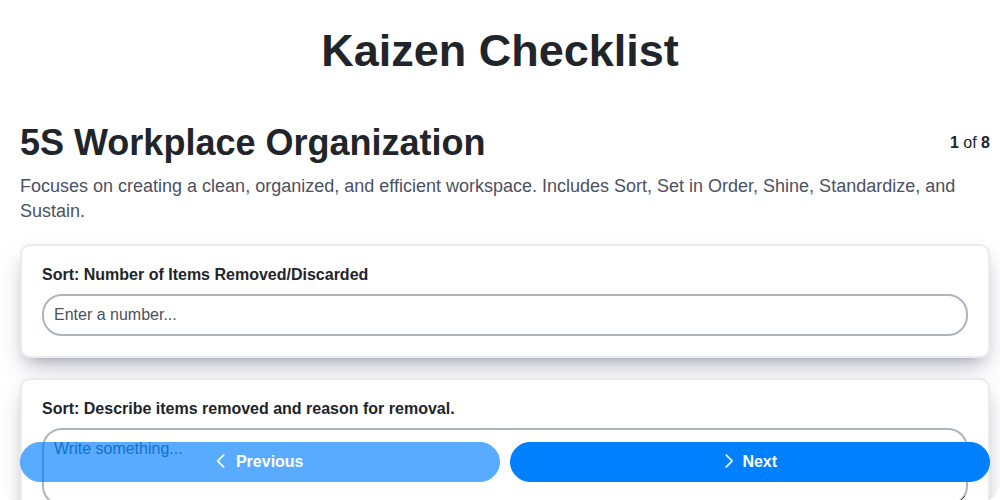
Шаблон за контролна листа Кайдзен: Вашият път към постоянно подобрение

Machine Safety Audit Checklist: Your Guide to a Safer Manufacturing Workplace
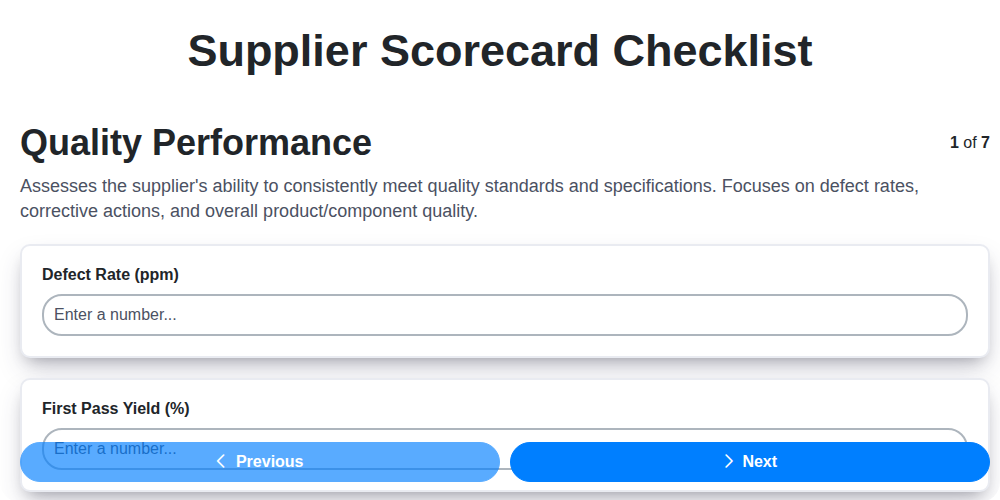
Mastering Supplier Performance: Your Free Supplier Scorecard Checklist Template
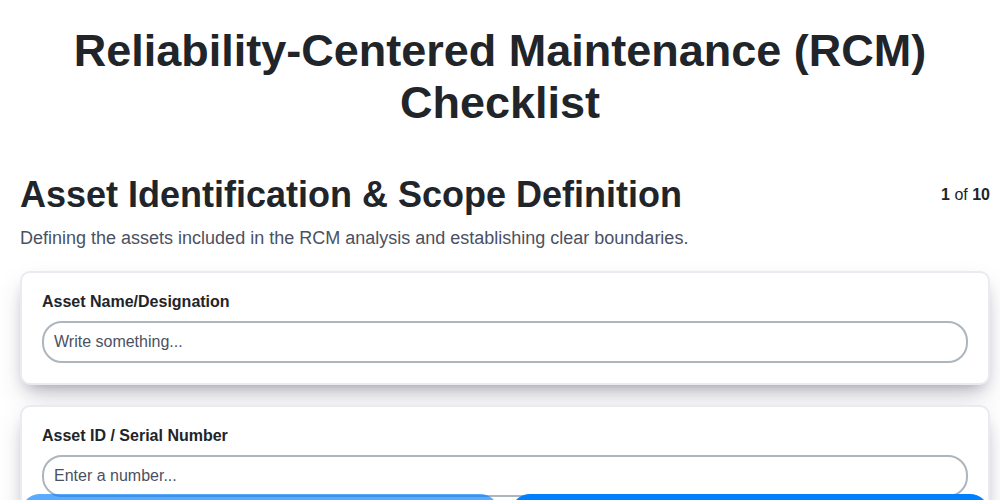
Your Ultimate RCM Checklist Template: A Step-by-Step Guide

Шаблон за контролен списък LPA: Вашето ръководство за слоести одити на процеси

Вашият краен шаблон за контролен списък за заключване/етикетиране (ЛОТО)

Your Ultimate FSC 22000 Checklist Template
Шаблон за проверка на качеството: Предотвратяване на дефекти и подобряване на производствените процеси
Можем да го направим заедно
Нуждаете се от помощ с
Производство?
Имате въпрос? Тук сме, за да помогнем. Моля, изпратете запитването си и ние ще отговорим своевременно.